题目内容
部分弱酸的电离平衡常数如下表:
弱酸 | H2CO3 | H2SO3 | HClO |
电离平衡常数 (25℃) | K1=4.30×10-7 K2=5.61×10-11 | K1=1.54×10-2 K2=1.02×10-7 | K=2.95×10-8 |
下列说法不正确的是( )
A.NaHSO3溶液中的离子浓度大小为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
B.相同温度时三种溶液的pH关系:Na2CO3>NaClO>Na2SO3
C.ClO-+CO2+H2O=HClO+HCO3-
D.2ClO-+SO2+H2O=2HClO+SO32-
练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
下图是元素周期表中短周期的一部分,X、Y、Z、W四种元素的原子核外最外层电子数之和等于Y、Z元素的原子序数之和。下列说法正确的是
X | Y | ||
Z | W |
A.X元素形成的气态氢化物分子的空间结构是三角形
B.Z与W元素形成的化合物是分子晶体
C.W单质受热蒸发时吸收的热量用于克服共价键
D.化合物XW3中W的化合价为-1价



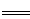 CO2(g)+2H2(g)△H= -bkJ•mol-1,则a_____b(填“>”、“<”或“=”)。
CO2(g)+2H2(g)△H= -bkJ•mol-1,则a_____b(填“>”、“<”或“=”)。 2NH3(g) ∆H= —92.4kJ•mol?1 一种工业合成氨的简易流程图如下:
2NH3(g) ∆H= —92.4kJ•mol?1 一种工业合成氨的简易流程图如下: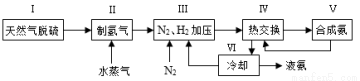
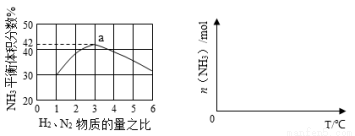
 N2(g)+2CO2(g),△H=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+2CO2(g),△H=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( ) Fe2++Cr3+.下列说法一定正确的是( )
Fe2++Cr3+.下列说法一定正确的是( )