题目内容
学习了影响化学反应速率的条件等知识后,高二3班的同学分组进行实验,对不同条件下的“锌与盐酸反应”进行探究,得到的结果如下表所示:组别 | 锌的质量/g | 锌的形状 | 温度/℃ | 溶解于酸所需的时间/s |
第一组 | 2 | 薄片 | 5 | 400 |
第二组 | 2 | 薄片 | 15 | 200 |
第三组 | 2 | 薄片 | 25 | 100 |
第四组 | 2 | 薄片 | 35 | 40 |
第五组 | 2 | 薄片 | 45 | 25 |
第六组 | 2 | 粉末 | 15 | 5 |
试求:
(1)画一幅以时间对温度的曲线图(纵轴表示时间,横轴表示温度)。
(2)利用所画的曲线图,关于温度影响反应速率你能得出什么结论?
(3)20 ℃时,2 g锌片溶解于酸中需多少时间?
(4)对比第二组与第六组实验,解释第六组实验反应为什么那么快。
思路解析:本题侧重在其他条件相同时,比较外界条件的改变对反应速率的影响,同时侧重对由表中信息转化为图中信息能力的考查。
答案:(1)如下图所示:

(2)对于该溶液,温度每升高10 ℃,反应速率加快到原来的2倍。
(3)约150 s。
(4)这是因为第二组中锌是块状,第六组中锌是粉末状,粉末状与酸溶液的接触面积要比块状大得多,从而使有效碰撞次数大大增多,加快了反应速率。

练习册系列答案
相关题目
学习了影响化学反应速率的条件等知识后高二(3)班的同学分组进行实验,对不同条件下的“锌与盐酸反应”进行探究,得到的结果如下表所示:
| 锌的质量/g | 锌的形状 | 温度/℃ | 溶解于酸所需的时间/s |
第一组 | 2 | 薄片 | 5 | 400 |
第二组 | 2 | 薄片 | 15 | 200 |
第三组 | 2 | 薄片 | 25 | 100 |
第四组 | 2 | 薄片 | 35 | 40 |
第五组 | 2 | 薄片 | 45 | 25 |
第六组 | 2 | 粉末 | 15 | 5 |
试求:(1)画一幅以时间对温度的曲线图(纵轴表示时间,横轴表示温度)。
(2)利用所画的曲线图,关于温度影响反应速率你能得出什么结论?
(3)20 ℃时,2 g锌片溶解于酸中需多少时间?
(4)对比结果第二组与第六组, 第六组为什么那么快?

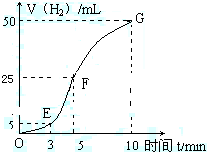 某课外兴趣小组欲探究铝与盐酸反应的能量变化以及影响化学反应速率的因素.做如下实验,请填写下列空白:
某课外兴趣小组欲探究铝与盐酸反应的能量变化以及影响化学反应速率的因素.做如下实验,请填写下列空白: