题目内容
已知:H2SO3的Ka1=1.54×10-2,Ka2=6.6×10-8;H2CO3的K′a1=4.2×10-7,K′a2=5.6×10-11,下列反应不能进行的是( )
| A、HSO3-+HCO3-=SO32-+H2CO3 |
| B、SO2+HCO3-=HSO3-+CO2 |
| C、HSO3-+CO32-=HCO3-+SO32- |
| D、2H2SO3 +CO32-=2HSO3-+CO2↑ |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:依据电离常数大小判断H2SO3、HSO3-、H2CO3、HCO3-酸性强弱,依据强酸制备弱酸的原理判断反应能否发生,据此解答.
解答:
解:H2SO3的Ka1=1.54×10-2,Ka2=6.6×10-8;H2CO3的K′a1=4.2×10-7,K′a2=5.6×10-11,所以H2SO3、HSO3-、H2CO3、HCO3-酸性由强到弱的顺序为:H2SO3、H2CO3、HSO3-、HCO3-,依据强酸制备弱酸的原理判断.
A.H2CO3酸性强于HSO3-,所以HSO3-+HCO3-=SO32-+H2CO3不正确,故A错误;
B.二氧化硫溶与水生成H2SO3,过量亚硫酸与碳酸氢根离子反应生成二氧化碳和亚硫酸氢根离子,故B正确;
C.HSO3-酸性强于HCO3-,所以HSO3-+CO32-=HCO3-+SO32-能够反应,故C正确;
D.H2SO3酸性强于H2CO3,2H2SO3 +CO32-=2HSO3-+CO2↑能够发生,故D正确;
故选:A.
A.H2CO3酸性强于HSO3-,所以HSO3-+HCO3-=SO32-+H2CO3不正确,故A错误;
B.二氧化硫溶与水生成H2SO3,过量亚硫酸与碳酸氢根离子反应生成二氧化碳和亚硫酸氢根离子,故B正确;
C.HSO3-酸性强于HCO3-,所以HSO3-+CO32-=HCO3-+SO32-能够反应,故C正确;
D.H2SO3酸性强于H2CO3,2H2SO3 +CO32-=2HSO3-+CO2↑能够发生,故D正确;
故选:A.
点评:本题考查了电离常数的应用,明确电离常数的意义是解题关键,题目难度不大.

练习册系列答案
相关题目
能作为潜水艇和呼吸面具中供氧剂的是( )
| A、MnO2 |
| B、Na2O2 |
| C、KMnO4 |
| D、KClO3 |
网易探索2010年5月20日报道,来自法国格勒诺布尔(Grenoble)约瑟夫命傅立叶大学的研究小组发明了第一块可为人体人造器官提供电能的可植入的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶的作用下发生了反应,已知其总反应为:C6H12O6+6O2=6CO2+6H2O(酸性环境),则下列对该电池说法不正确的是( )
| A、消耗1mol氧气时转移4mole-,H+向正极移动 |
| B、电池负极的反应为:C6H12O6+6H2O-24e-=6CO2+24H+ |
| C、今后的研究方向是怎样提高葡萄糖生物燃料电池的效率,从而达到可以利用葡萄糖生物燃料电池为任何可植入医疗设备提供电能 |
| D、该生物燃料电池可以在高温下工作 |
下列实验装置不能达到预期目的是( )


| A、装置①用于测定H2O2分解的反应速率 |
| B、装置②用于证明元素的非金属性:S>C>Si |
| C、装置③用于证明Na2CO3的水解是吸热反应 |
| D、装置④用于测定中和热 |
下列实验装置或对实验现象的描述正确的是( )
A、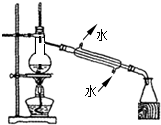 分馏装置 |
B、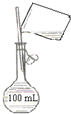 配制150 mL 0.10 mol?L-1盐酸 |
C、 烧瓶内溶液变蓝色 |
D、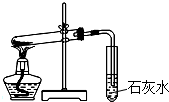 探究NaHCO3的热稳定性 |
下列仪器中,需要垫石棉网加热的是( )
A、 |
B、 |
C、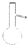 |
D、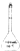 |
下列叙述错误的是( )
| A、用金属钠可区分乙醇和乙醚 |
| B、用高锰酸钾酸性溶液可区分己烷和3-己烯 |
| C、用水可区分苯和溴苯 |
| D、用饱和氢氧化钾乙醇溶液、硝酸银溶液可以检验1-氯丙烷中含有氯元素 |

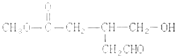
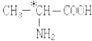 ,有机物A的结构简式如图所示:
,有机物A的结构简式如图所示: