题目内容
17.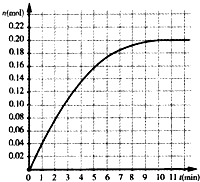 恒温条件下,往容积为2L的密闭容器内加入0.4mol的N2和1.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g),反应中NH3物质的量变化情况如图:下列说法不合理的是( )
恒温条件下,往容积为2L的密闭容器内加入0.4mol的N2和1.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g),反应中NH3物质的量变化情况如图:下列说法不合理的是( )| A. | 其它条件不变,若改用5L容器达到平衡需要的时间将大于10min | |
| B. | N2平衡转化率为25% | |
| C. | 平衡时气体总压强为开始时的90% | |
| D. | 反应前10min反应速率v(H2)=0.01mol?L-1?min-1 |
分析 A.体积变大浓度减小,反应速率减慢,达平衡所需时变长;
B. N2(g)+3H2(g)?2NH3(g)
起始量(mol):0.4 1.6 0
变化量(mol):0.1 0.3 0.2
平衡量(mol):0.3 1.3 0.2
转化率=$\frac{消耗量}{起始量}$×100%;
C.根据三行式计算平衡气体物质的量,结合平衡时气体和起始气体压强之比等于气体物质的量之比;
D.根据公式v=$\frac{△c}{△t}$,结合速率之比等于对应物质的化学计量数之比进行求解.
解答 解:A.体积变大浓度减小,反应速率减慢,达平衡所需时变长,所以平衡需要的时间大于l0min,故A正确;
B. N2(g)+3H2(g)?2NH3(g)
起始量(mol):0.4 1.6 0
变化量(mol):0.1 0.3 0.2
平衡量(mol):0.3 1.3 0.2
所以N2平衡转化率为:$\frac{0.1mol}{0.4mol}$×100%=25%,故B正确;
C.平衡时气体总压强为开始时压强的倍数为:$\frac{0.3+1.3+0.2}{0.4+1.6}$×100%=90%,故C正确;
D.反应前l0min反应速率v(NH3)=$\frac{\frac{0.2mol}{2L}}{10min}$=0.01mol•L-1•min-1,所以v(H2)=$\frac{3}{2}$v(NH3)=$\frac{3}{2}$×0.01mol•L-1•min-1=0.015mol•L-1•min-1,故D错误;
故选D.
点评 本题考查求化学反应的速率、转化率、体积分数和影响速率的因素,学生只要抓住公式就可以求解,综合性强,题目难度中等.

| A. | 吸水性 | B. | 脱水性 | C. | 强氧化性 | D. | 酸性 |
| A. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、I- | |
| B. | 水电离的H+浓度为1×10-13mol•L-1的溶液中,K+、Al3+、Cl-、SO42- | |
| C. | AlO2?浓度为0.1 mol•L-1的溶液中:Na+、K+、HCO3-、Cl- | |
| D. | 加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、NO3- |
| A. | pH=1的溶液:K+、Cu2+、Br-、SO42- | |
| B. | 含有0.1 mol•L-1I-的溶液:NH4+、Fe3+、SO42-、Cl- | |
| C. | 含有0.1 mol•L-1HCO3-的溶液:Na+、Al3+、NO3-、OH- | |
| D. | 强酸性溶液:K+、Mg2+、NO3-、ClO- |
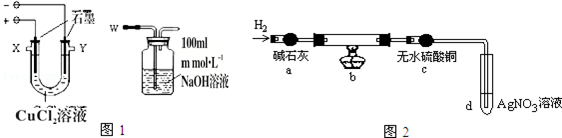
(1)导气管W端应与出气口X连接(填“X”或“Y”).
(2)实验后发现阴极碳棒上除了附着有红色物质,还附着有少量白色物质.查阅资料显示:
| 物质名称及化学式 | 氯化亚铜CuCl | 碱式氯化铜Cu2(OH)3Cl |
| 性质 | 白色固体、不溶水 | 绿色固体、不溶水 |
②红色物质可能有Cu;或者Cu2O;或者二者混合物.
实验Ⅱ为探究阴极碳棒上附着的红色、白色物质,设计了如下实验:取出阴极碳棒,洗涤、干燥、称其质量为W1g,并将其放入图2所示装置b中,进行实验.
实验中,碳棒上的白色物质完全变为红色,无水硫酸铜不变色,d中出现白色沉淀;实验结束时,继续通H2直至碳棒冷却后,称量其质量为W2g.
(3)无水硫酸铜的作用是检验红色物质中有无Cu2O.
(4)装置b中发生反应的化学方程式是2CuCl+H2=2Cu+2HCl.
(5)电解CuCl2溶液时,阴极上产生白色物质的原因为(用电极反应式解释)Cu2++e-+Cl-=CuCl↓;阴极上产生白色物质的物质的量是$\frac{W{\;}_{1}-W{\;}_{2}}{35.5}$mol.
实验Ⅲ测定漂白液中NaClO的浓度:准确移取20.00mL洗气瓶内混合溶液,加入适量的H2O2溶液,摇匀,滴加2~3滴酚酞试液,用 n mol•L-1盐酸滴定至终点,消耗盐酸V mL.
(6)用化学方程式表示加入H2O2溶液的作用NaClO+H2O2=O2↑+NaCl+H2O.
(7)若忽略洗气瓶内的副反应及体积变化,漂白液中NaClO的浓度为$\frac{20m-nV}{40}$mol•L-1.
| A. | 标准状况下,1mol H2完全燃烧生成气态水放出285.8kJ热量,则H2的燃烧热为-285.8kJ•mol-1 | |
| B. | 测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度,NaOH起始温度和反应后最高温度 | |
| C. | 在101 kPa时,1mol C与适量O2反应生成1mol CO时,放出110.5kJ热量,则C的燃烧热为110.5kJ•mol-1 | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.31 kJ•mol-1.若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3kJ |
| A. | 液氨可做致冷剂 | |
| B. | 二氧化硅可作为半导体材料 | |
| C. | 氢氧化铝常用于中和胃酸 | |
| D. | 常温下,铁制容器常用于盛装浓硫酸 |
| A. | 浓HCl、浓H2SO4、浓HNO3均具有氧化性,都属氧化性酸 | |
| B. | 根据分散系是否有丁达尔效应将分散系分为溶液、胶体和浊液 | |
| C. | NaOH、HNO3、NaNO3在水溶液中均能电离出离子,都属离子化合物 | |
| D. | Na2O2、HCl、BaSO4在熔融状态或溶于水时均能导电,都属电解质 |