题目内容
用双线桥法表示下列氧化还原反应
Zn+H2SO4(稀)
Zn SO4+H2↑
MnO2+4H Cl(浓)
MnCl2+Cl2↑+2H2O
C+2CuO
Cu+CO2↑
Fe2O3+3CO
Fe+3CO2. .
Zn+H2SO4(稀)
| ||
MnO2+4H Cl(浓)
| ||
C+2CuO
| ||
Fe2O3+3CO
| ||
考点:氧化还原反应
专题:氧化还原反应专题
分析:反应Zn+H2SO4═ZnSO4+H2↑中,Zn元素化合价升高,被氧化,为还原剂,H元素化合价降低,被还原,H2SO4为氧化剂,转移2e-;
MnO2+4H Cl(浓)
MnCl2+Cl2↑+2H2O中,锰元素化合价降低,氯元素化合价升高,转移电子数为2mol;
CuO+CO
Cu+CO2中,氧化铜中Cu的化合价由+2价降到0价,一氧化碳中C的化合价由+2升高到+4价;
Fe2O3+3CO
2Fe+3CO2 反应中,Fe元素的化合价由+3降低为0,C元素的化合价由+2升高为+4价,以此来解答.
MnO2+4H Cl(浓)
| ||
CuO+CO
| ||
Fe2O3+3CO
| ||
解答:
解:Zn+H2SO4(稀)
ZnSO4+H2↑中,Zn元素的化合价升高,H元素非化合价降低,转移的电子数为2e-,电子转移的方向和数目为 ,
,
MnO2+4H Cl(浓)
MnCl2+Cl2↑+2H2O中,锰元素化合价降低,氯元素化合价升高,转移电子数为2mol,用“双线桥法”表示氧化还原反应中电子转移情况为: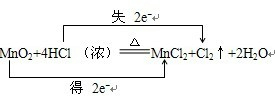 ;
;
CuO+CO
Cu+CO2中,氧化铜中Cu的化合价由+2价降到0价,一氧化碳中C的化合价由+2升高到+4价,一氧化碳是还原剂,氧化铜为氧化剂,双线桥法为: ;
;
Fe2O3+3CO
2Fe+3CO2 反应中,Fe元素的化合价由+3降低为0,C元素的化合价由+2升高为+4价,该反应中3molCO参加反应,转移6mol电子,则双线桥表示该反应电子转移的方向和数目为为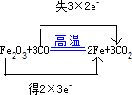 ,
,
故答案为: ;
; ;
; ;
; .
.
| ||
 ,
,MnO2+4H Cl(浓)
| ||
 ;
;CuO+CO
| ||
 ;
;Fe2O3+3CO
| ||
 ,
,故答案为:
 ;
; ;
; ;
; .
.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应电子转移方向和数目的考查,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
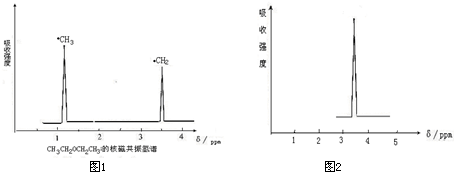
| A、C6H5CH2OH不属于醇类 |
| B、l mol苯最多能与3 mol H2加成,说明每个苯分子有3个碳碳双键 |
| C、苯和甲苯都能使KMnO4酸性溶液褪色 |
| D、1-氯丙烷和2-氯丙烷分别与NaOH乙醇溶液共热的反应产物相同 |
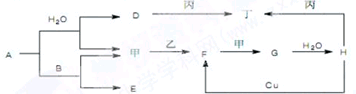
 【物质结构与性质】
【物质结构与性质】