题目内容
13.联氨(N2H4)及其衍生物是一类重要的火箭燃料.N2H4与N2O4反应能放出大量的热.(1)已知:2NO2(g)?N2O4(g),N2O4为无色气体.
①在上述条件下反应能够自发进行,则反应的△H<0(填写“>”、“<”、“=”)
②一定温度下,在密闭恒容容器中反应2NO2(g)?N2O4(g)达到平衡,达到平衡状态的标志ACE.
A.单位时间内消耗n molN2O4的同时生成2nmolNO2
B.用NO2、N2O4的物质的量浓度变化表示的反应速率之比为2:1的状态
C.混合气体的颜色不再改变的状态
D.混合气体的密度不再改变的状态
E.混合气体的平均相对分子质量不再改变的状态
③其他条件不变时,下列措施能提高NO2转化率的是BC(填字母)
A.增大NO2的浓度 B.降低温度 C.减小压强 D.加入催化剂
(2)25℃时,1molN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放612.5kJ的热量.
请写出该反应的热化学方程式:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)△H=-1225KJ/mol.
(3)17℃、1.01×105Pa,往10L密闭容器中充入NO2,达到平衡时,n(NO2)=0.2mol,n(N2O4)=0.16mol.则反应初始时,充入NO2的物质的量为3.4;该温度下反应N2O4(g)?2NO2(g)的平衡常数K为0.25.
分析 (1)①△H-T△S<0的反应能够自发进行;
②可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析;
③平衡正向移动可以通过反应物的转化率;
(2)根据热化学方程式的意义以及热化学方程式的书写方法来写;
(3)依据化学平衡三段式列式计算起始量,依据平衡浓度结合平衡常数概念计算得到,逆反应的平衡常数和正反应的平衡常数成倒数计算.
解答 解:(1)△H-T△S<0的反应能够自发进行,该反应△S<0,若反应能够自发进行,△H必须小于0,故答案为:<;
②A、生成n mol N2O4的同时生成2nmolNO2,说明正逆反应速率相等,反应达到平衡状态,故A正确;
B、速率之比等于化学计量数之比,不能说明反应达到平衡状态,故B错误;
C、颜色不变,说明二氧化氮的浓度不变,反应达到平衡状态,故C正确;
D、密度始终不变,所以密度不变不能说明反应达到平衡状态,故D错误;
E、平均相对分子质量不再改变,说明气体物质的量不变,反应达到平衡状态,故E正确;
故选ACE;
③A、减小二氧化氮的浓度,平衡逆向移动,其转化率减小,故A错误;
B、降低温度平衡向正向移动,其转化率增大,故B正确;
C、增大压强平衡正向移动,其转化率增大,故C正确;
D、升高温度,平衡逆向移动,其转化率减小,故D错误;
故选BC;
(2)1molN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放612.5kJ的热量,其热化学方程式为2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)△H=-1225KJ/mol,故答案为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)△H=-1225KJ/mol;
(3)17℃、1.01×105Pa,往10L密闭容器中充入NO2,达到平衡时,c(NO2)=0.2mol•L-1、c(N2O4)=0.16mol•L-1,反应初始时,充入NO2的物质的量浓度为0.34mol/L,n(NO2)=C(NO2)•V=0.34mol/L×10L=3.4mol;
该反应的平衡常数K=$\frac{0.16}{0.{2}^{2}}$=4mol-1/L-1该温度下反应N2O4(g)?2NO2(g)的平衡常数K′=$\frac{1}{K}$=0.25mol/L;
故答案为:3.4mol;0.25.
点评 本题考查范围广,难度大,需要对反应自发进行的条件、平衡移动转化率知识熟练掌握.

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
| A. | 若甲是C,则乙可能是O2 | B. | 若甲是Fe,则乙可能是Cl2 | ||
| C. | 若甲是NaOH溶液,则乙可能是SO2 | D. | 若甲是H2S,则乙可能是O2 |
| A. | 中和滴定盛待测液的锥形瓶中有少量水对滴定结果无影响,锥形瓶不能用待测液润洗 | |
| B. | 酸式和碱式滴定管用蒸馏水洗净后还需用标准液或待测液润洗 | |
| C. | 滴定时左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视锥形瓶中颜色变化 | |
| D. | 滴定前仰视读数,滴定后平视刻度读数,被测待测溶液偏高 |
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的H2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀. |
(1)实验目的:研究同周期元素性质递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制H2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等.
仪器:①烧杯,②试管,③酒精灯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式及此实验的结论)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
(4)请你补充一组实验方案(简单易行),证明此周期中另两种主族元素的性质递变规律.向硅酸钠溶液中加入磷酸溶液,有白色沉淀生成,说明磷酸的酸性比硅酸强,即非金属性:P>Si.
| A. | 锕系元素 | B. | 金属元素 | C. | 镧系元素 | D. | 第六周期元素 |
| A. | pH=2 的H2C2O4 溶液与pH=12 的NaOH 溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+c(C2O42-) | |
| B. | 0.1 mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) | |
| C. | 硫酸氢铵溶液中滴加氢氧化钠至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) | |
| D. | pH相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液:c[(NH4)2SO4]<c[(NH4)2Fe(SO4)2]<c(NH4Cl) |
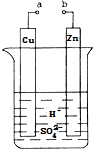 原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置:
原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置: