题目内容
25℃时,下列各组离子在指定溶液中能大量共存的是( )
| A、pH=11的溶液中:Na+、K+、MnO4-、CO32- |
| B、滴入酚酞显红色的溶液中:Na+、Al3+、AlO2-、NO3- |
| C、0.1mol/L NH4HCO3 溶液中:Na+、Al3+、NO3-、Cl- |
| D、0.1mol/L FeCl3溶液中:Fe2+、NH4+、SCN-、SO42- |
考点:离子共存问题
专题:
分析:A.pH=11的溶液呈碱性;
B.滴入酚酞显红色的溶液呈碱性,和OH-反应的离子不能大量共存;
C.NH4HCO3溶液中不能大量存在和HCO3-或NH4+反应的离子;
D.氯化铁溶液中不能大量存在和铁离子或氯离子反应的离子.
B.滴入酚酞显红色的溶液呈碱性,和OH-反应的离子不能大量共存;
C.NH4HCO3溶液中不能大量存在和HCO3-或NH4+反应的离子;
D.氯化铁溶液中不能大量存在和铁离子或氯离子反应的离子.
解答:
解:A.pH=11的溶液呈碱性,这几种离子之间不反应,且和氢氧根离子不反应,所以能大量共存,故A正确;
B.滴入酚酞显红色的溶液呈碱性,Al3+和OH-反应生成Al(OH)3沉淀而不能大量共存,Al3+、AlO2-发生双水解反应而不能大量共存,故B错误;
C.NH4HCO3溶液中,HCO3-或Al3+发生双水解反应而不能大量共存,故C错误;
D.Fe3+、SCN-生成络合物而不能大量共存,故D错误;
故选A.
B.滴入酚酞显红色的溶液呈碱性,Al3+和OH-反应生成Al(OH)3沉淀而不能大量共存,Al3+、AlO2-发生双水解反应而不能大量共存,故B错误;
C.NH4HCO3溶液中,HCO3-或Al3+发生双水解反应而不能大量共存,故C错误;
D.Fe3+、SCN-生成络合物而不能大量共存,故D错误;
故选A.
点评:本题考查离子共存,为高考高频点,涉及双水解反应、络合反应、复分解反应等知识点,明确离子性质及离子共存条件即可解答,题目难度不大.

练习册系列答案
相关题目
下列试剂的保存方法正确的是( )
| A、NaOH溶液保存在配有玻璃塞的细口瓶中 |
| B、金属钠通常密封保存在煤油中 |
| C、氯水保存在无色透明的试剂瓶中 |
| D、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
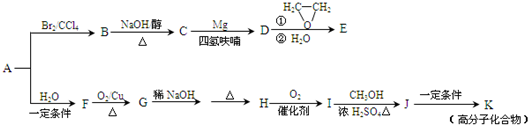
已知,有机化合物A只由碳、氢两种元素组成且能使溴水褪色,其产量可以用来衡量一个国家石油化工发展水平.A、B、C、D、E有如下关系:则下列推断不正确的是( )


| A、B+D→E的化学方程式为:CH3CH2OH+CH3COOH→CH3COOC2H5 |
| B、D中含有的官能团为羧基,利用D物质可以清除水壶中的水垢 |
| C、物质C的结构简式为CH3CHO,E的名称为乙酸乙酯 |
| D、鉴别A和甲烷可选择使用酸性高锰酸钾溶液 |
X、Y、Z、W均为中学化学中常见物质,一定条件下它们之间有如图转化关系(其它产物已略去):下列说法不正确的是( )
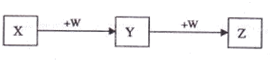

| A、若W是单质铁,则Z溶液可能是FeCl2溶液 |
| B、若W是氢氧化钠,则X水溶液呈酸性 |
| C、若W是氧气,则X、Z的相对分子质量可能相差48 |
| D、若W是强氧化性的单质,则X可能是金属铝 |
关于溴乙烷与NaOH的乙醇溶液反应说法正确的是( )
| A、该反应是溴乙烷的水解反应 |
| B、往反应后的溶液中直接加入AgNO3溶液检验是否有Br-生成 |
| C、该反应产物中有水、钠盐和不饱和烃 |
| D、生成的气体可直接通入到溴水中检验是否有乙烯生成 |
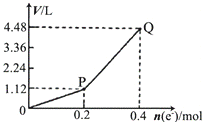 用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如图所示.横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).下列判断正确的是( )
用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如图所示.横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).下列判断正确的是( )| A、电解过程中,溶液的pH不断增大 |
| B、当转移0.4mol e-时,电解生成的铜为6.4g |
| C、阳极电极反应式为2H2O+4e-=4H++O2↑ |
| D、Q点对应的气体中,H2与O2的体积比为2:1 |
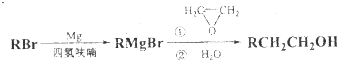
 实验室要测定某氯化铜溶液中溶质的质量分数,取该溶液100g,逐滴滴加一定溶质质量分数的氢氧化钠溶液,反应过程中生成沉淀的质量与加入氢氧化钠溶液质量的关系如图所示.(反应的化学方程式:2NaOH+CuCl2=Cu(OH)2↓+2NaCl)求:
实验室要测定某氯化铜溶液中溶质的质量分数,取该溶液100g,逐滴滴加一定溶质质量分数的氢氧化钠溶液,反应过程中生成沉淀的质量与加入氢氧化钠溶液质量的关系如图所示.(反应的化学方程式:2NaOH+CuCl2=Cu(OH)2↓+2NaCl)求: