题目内容
A、B两元素的原子分别得到2个电子形成稳定结构时,A放出的能量大于B放出的能量;C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量.若A、B、C、D间分别形成化合物时,属于离子化合物可能性最大的是( )
| A、D2A |
| B、C2B |
| C、C2A |
| D、D2B |
考点:原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:A、B两元素的原子分别获得两个电子形成稳定结构时,A放出的能量大于B放出的能量.说明A得电子的能量强于B,非金属性比B强;
C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量.说明C失电子的能力比D高,金属性比D高.
C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量.说明C失电子的能力比D高,金属性比D高.
解答:
解:得电子形成稳定结构放出的能量越多,说明元素原子越易得电子,元素的非金属性越强,同理,失电子形成稳定结构吸收的能量越多,说明元素原子越难失电子,元素的金属性越弱,
A、B两元素的原子分别获得两个电子形成稳定结构时,A放出的能量大于B放出的能量.说明A得电子的能量强于B,则A的非金属性比B强;
C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量.说明C失电子的能力比D高,则C的金属性比D强,
因此,A、C之间最易形成离子化合物.
故选C.
A、B两元素的原子分别获得两个电子形成稳定结构时,A放出的能量大于B放出的能量.说明A得电子的能量强于B,则A的非金属性比B强;
C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量.说明C失电子的能力比D高,则C的金属性比D强,
因此,A、C之间最易形成离子化合物.
故选C.
点评:本题考查原子的结构与元素周期律的关系,题目难度不大,注意原子得失电子与能量的大小关系和非金属性、金属性强弱的联系.

练习册系列答案
相关题目
下列有关实验原理、操作或现象不正确的是( )
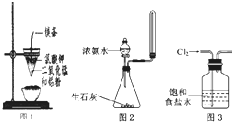

| A、图1装置可制得金属锰,用同样的装置可制得金属铬 |
| B、实验室用图2所示装置制取少量纯净的氨气 |
| C、用玻璃棒蘸取某溶液做焰色反应实验,火焰呈黄色不能说明该溶液中含有钠元素 |
| D、实验室用图3所示装置除去Cl2中的少量HCl |
检验SO42-的存在,最好选用下列物质中的( )
| A、石蕊溶液 | B、碳酸钠溶液 |
| C、硝酸溶液 | D、氯化钡溶液 |
由一种阳离子与两种酸根离子组成的盐称为混盐.混盐CaOCl2在酸性溶液中可以产生Cl2,下列关于混盐CaOCl2的有关判断正确的是(NA为阿伏加德罗常数)( )
| A、该混盐在酸性溶液中产生1 molCl2时转移的电子数为2NA |
| B、该混盐的水溶液显碱性 |
| C、该混盐中氯元素的化合价为-1价 |
| D、该混盐具有较强的还原性 |
在下列各组物质中,一定互为同系物的是( )
| A、符合通式CnH2n+2,且相对分子质量不相等的两种有机化合物 |
| B、符合通式CnH2n-2,且相对分子质量不相等的两种有机化合物 |
| C、符合通式CnH2n-6,且相对分子质量不相等的两种有机化合物 |
| D、符合通式CnH2n,且相对分子质量不相等的两种有机化合物 |
在含有Na+、Cl-、K+、SO42-的混合溶液中,测得c(Na+)=1mol/L,c(K+)=2mol/L,c(Cl-)=2mol/L,则c(SO42-)等于( )
| A、0.5mol/L |
| B、1mol/L |
| C、1.5mol/L |
| D、2mol/L |
等质量的铝分别与足量的稀盐酸和氢氧化钠溶液反应,两个反应放出的气体在相同状况下体积比为( )
| A、3:1 | B、2:1 |
| C、1:1 | D、1:3 |
下列溶液中的Cl-数目与50mL 1mol/L的AlCl3溶液中Cl-数目相等的是( )
| A、150mL 1mol/L的NaCl |
| B、75mL 1mol/L的FeCl3 |
| C、150mL 3mol/L的KCl |
| D、75mL 2mol/L的CaCl2 |