题目内容
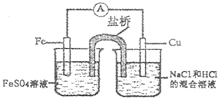 根据下图判断,下列正确的说法是( )
根据下图判断,下列正确的说法是( )分析:Fe比Cu活泼,为原电池的负极,发生Fe-2e-═Fe2+,Cu为正极,发生还原反应,电极方程式为2H++2e-=H2↑,原电池工作时,阳离子向正极移动,阴离子向负极移动,以此解答该题.
解答:解:A.负极发生氧化反应,铁被氧化,电极方程式为Fe-2e-═Fe2+,故A正确;
B.Cu为正极,发生还原反应,电极方程式为2H++2e-=H2↑,故B错误;
C.放电过程中,右侧烧杯中消耗氢离子,溶液的pH增大,故C正确;
D.盐桥中的阳离子向正极,即右侧移动,故D错误.
故选AC.
B.Cu为正极,发生还原反应,电极方程式为2H++2e-=H2↑,故B错误;
C.放电过程中,右侧烧杯中消耗氢离子,溶液的pH增大,故C正确;
D.盐桥中的阳离子向正极,即右侧移动,故D错误.
故选AC.
点评:本题考查原电池知识,侧重于学生的分析能力和电化学知识的综合考查,为高考常见题型和高频考点,注意根据电极方程式的书写,难度不大.

练习册系列答案
相关题目
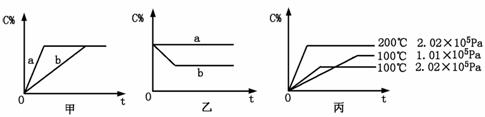
 xC(g)的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
xC(g)的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。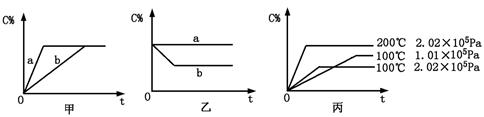
 xC(g)的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
xC(g)的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。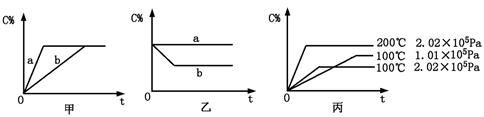
 xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图: 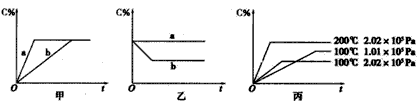
 CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题: