题目内容
8.如表是周期表中的一部分,根据A-K在周期表中的位置,用元素符号或化学式回答.| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H | ||||
| 4 | J | K |
(2)最高价氧化物的水化物碱性最强的是KOH,酸性最强的是HClO4,呈两性的是Al(OH)3.
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的HF,
(4)在这些元素中(除I外),原子半径最大的是K,原子半径最小的是F
(5)D和K组成化合物的电子式
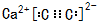 ,
,(6)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式:Al2O3+2OH-=2AlO2-+2H2O.
分析 根据元素在周期表中的位置知,A-K分别是H、Na、Al、C、N、P、F、Cl、Ne、K、Ca元素,
(1)化学性质最不活泼的元素是0族元素,只有负化合价没有正化合价的元素为最活泼的非金属元素;氧化性最强的元素是非金属性最强的元素,还原性最强的元素是金属性最强的元素;
(2)元素的金属性越强,其最高价氧化物的水化物碱性越强;元素的非金属性越强,其最高价氧化物的水化物酸性越强,但O、F元素除外;
(3)元素的非金属性越强,其氢化物的稳定性越强;
(4)原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
(5)D和K组成的化合物是碳化钙,为离子化合物;
(6)B的最高价氧化物的水化物是NaOH、C的最高价氧化物是氧化铝,二者反应生成偏铝酸钠和水.
解答 解:根据元素在周期表中的位置知,A-K分别是H、Na、Al、C、N、P、F、Cl、Ne、K、Ca元素,
(1)化学性质最不活泼的元素是0族元素,则这几种元素化学性质最不活泼的是Ne;只有负化合价没有正化合价的元素为最活泼的非金属元素,为F元素;氧化性最强的元素是非金属性最强的元素,为F元素,氧化性最强的单质是F2,还原性最强的元素是金属性最强的元素,为K元素,
故答案为:Ne;F;F2;K;
(2)元素的金属性越强,其最高价氧化物的水化物碱性越强;元素的非金属性越强,其最高价氧化物的水化物酸性越强,但O、F元素除外,这几种元素金属性最强的是K、除了F元素外非金属性最强的是Cl元素,所以最高价氧化物的水化物碱性最强的是KOH,酸性最强的是HClO4,呈两性的是Al(OH)3,
故答案为:KOH;HClO4;Al(OH)3;
(3)元素的非金属性越强,其氢化物的稳定性越强,这几种元素中非金属性最强的是F元素,则形成的氢化物稳定性最强的是HF,故答案为:HF;
(4)原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,这些元素中原子半径最大的是K,最小的是F,故答案为:K;F;
(5)D和K组成的化合物是碳化钙,为离子化合物,电子式为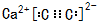 ,故答案为:
,故答案为: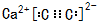 ;
;
(6)B的最高价氧化物的水化物是NaOH、C的最高价氧化物是氧化铝,二者反应生成偏铝酸钠和水,离子方程式为Al2O3+2OH-=2AlO2-+2H2O,故答案为:Al2O3+2OH-=2AlO2-+2H2O.
点评 本题考查位置结构性质的相互关系及运用,涉及离子方程式的书写、电子式的书写、元素周期律等知识点,侧重考查学生对化学用语的掌握及运用,把握元素周期律是解本题关键,注意规律中的异常现象,会正确书写碳化钙的电子式,题目难度不大.

| A. | 用丁达尔效应分离Fe(OH)3胶体和FeCl3溶液 | |
| B. | Fe(OH)3胶体的胶粒带正电荷,通电时胶粒向直流电源的负极移动,这种现象称为电泳 | |
| C. | 向沸腾蒸馏水逐滴加饱和FeCl3溶液,至液体呈透明红褐色时即得到Fe(OH)3胶体 | |
| D. | 向沸腾的NaOH稀溶液中边滴加FeCl3饱和溶液,边用玻璃棒搅动,然后继续煮沸,制备Fe(OH)3胶体 |
| A. | Cu | B. | Fe | C. | Al | D. | Mg |
| A. | BaCl2、稀硝酸 | B. | AgNO3、稀硝酸 | C. | 稀盐酸、BaCl2 | D. | AgNO3、稀盐酸 |
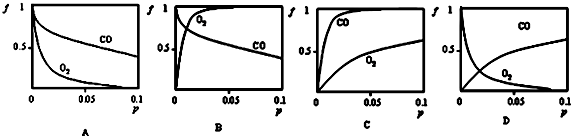

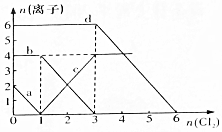 已知Cl-、Br-、Fe2+、I-的还原性依次增强.现向FeBr2、FeI2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示,请回答:
已知Cl-、Br-、Fe2+、I-的还原性依次增强.现向FeBr2、FeI2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示,请回答: