题目内容
12.下列关于硅及其化合物叙述中,正确的是( )| A. | CO2和SiO2都能与水反应生成相应的酸 | |
| B. | 硅可以用做半导体材料,SiO2可用于制光导纤维 | |
| C. | 氢氧化钠溶液保存在磨口玻璃塞的试剂瓶中 | |
| D. | 玻璃是人类最早使用的硅酸盐材料,玻璃加热熔化时有固定的熔点 |
分析 A.二氧化硅不溶于水;
B.硅处于金属和非金属元素之间,其单质是良好的半导体材料;光导纤维的主要成分是二氧化硅;
C.玻璃中含有二氧化硅,二氧化硅是酸性氧化物,能和氢氟酸、强碱溶液反应;
D.人类最早使用的硅酸盐材料是陶瓷,晶体有固定熔点,非晶体没有熔点,玻璃是硅酸盐,没有固定的熔点;
解答 解:A.二氧化硅不溶于水,不能与水反应生成硅酸,故A错误;
B.硅处于金属和非金属元素之间,具有金属和非金属的性质,所以其单质是良好的半导体材料;光导纤维的主要成分是二氧化硅,是利用光的全反射原理,故B正确;
C.玻璃中含有二氧化硅,二氧化硅和氢氧化钠溶液生成粘性的硅酸钠不便于打开,所以不能用玻璃塞,故C错误;
D.人类最早使用的硅酸盐材料是陶瓷,玻璃是硅酸盐,因玻璃是玻璃态物质,是混合物,没有固定的熔点,故D错误;
故选B.
点评 本题考查硅及其化合物的性质和用途,明确物质的性质是解本题关键,题目难度不大..

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表:下列说法不正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 012 | 011 | 010 | 010 |
| A. | 反应前2min的平均速率v(Z)=2.0×10-5 mol•L-1•min-1 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前:v(逆)>v(正) | |
| C. | 该温度下此反应的平衡常数:K=1.44 | |
| D. | 保持其他条件不变,起始时向容器充入0.32 mol气体X和0.32mol气体Y,到达平衡时,n(Z)=0.024mol |
13.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 5.6gFe在氧气中燃烧,完全反应时转移电子数为0.3NA | |
| B. | 1L 0.1mol•L-1AlC13中所含Al3+离子数小于0.1NA | |
| C. | 1LpH=1的H2SO4溶液中含有的H+数为0.2NA | |
| D. | 常温下,1.7gNH3和3.65gHCl混合后,气体分子数为0.2NA |
7.可逆反应N2(g)+3H2(g)?2NH3(g)在密闭容器中进行,一段时间后测得c(N2)=1.5mol/L,c(H2)=0.6mol/L,c(NH3)=1.5mol/L,则此反应达到平衡后,下列数据可能正确的是( )
| A. | c(N2)=2.25 mol/L | B. | c(NH3)=1.9 mol/L | C. | c(H2)=0.3 mol/L | D. | c(N2)=1.3mol/L |
17.有关氢氧燃料电池的电极反应,下列说法正确的是( )
| A. | 电解质为NaCl溶液,正极反应为H2+2e-=2H+ | |
| B. | 电解质为NaOH溶液,正极反应为O2+2e-=2OH- | |
| C. | 电解质为HCl溶液,正极反应为O2+4e-+4H+=2H2O | |
| D. | 电解质为Na2CO3溶液,正极反应为H2+2e-+CO32-=H2O+CO2↑ |
4.FeCl2是一种常用的还原剂.有关数据如下:
查阅资料知:氯化铁遇水剧烈水解.实验室可以用如下方法来制备无水FeCl2.
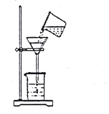
按图装置,在三颈烧瓶中放入a g无水氯化铁和过量的氯苯,控制反应温度在128~139℃加热3h,冷却,分离提纯得到粗产品.

回答下列问题:
(1)上述生成FeCl2的反应中,还原剂是C6H5Cl.
(2)实验装置中,仪器B的作用是防止安全瓶内的水分进入A装置,导致FeCl2变质,虚线框内应选择的安全瓶(盛有蒸馏水)是c.(填标号)
(3)实验过程中控制反应温度接近或超过C6H5Cl的沸点,C6H5Cl不会有明显损失,原因是_实验使用了冷凝回流装置.
(4)冷却反应后的实验装置,对三颈烧瓶内的物质进行过滤、洗涤、干燥,得到粗产品.
①洗涤沉淀所用的试剂应为b.(填标号)
a.蒸馏水 b.苯 c.烧碱溶液
②回收滤液中C6H5Cl的方案为蒸馏滤液,并收集132℃馏分.
(5)用x mol•L-1NaOH溶液滴定安全瓶中得到的盐酸,消耗少y mLNaOH溶液,则反应中氯化铁的转化率为$\frac{x•y×1{0}^{-3}×2×162.5}{a}×100%$(只列出计算式).
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38此温度下在实验室中配制100mL5.0mol•L-1,FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入2mol•L-1的盐酸2.5mL(总体积忽略加入盐酸体积).
| C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl、C6H4Cl2、苯,易吸水. | ||
| 熔点/℃ | -45 | 53 | -- | -- |
| 沸点/℃ | 132 | 173 | -- | -- |
按图装置,在三颈烧瓶中放入a g无水氯化铁和过量的氯苯,控制反应温度在128~139℃加热3h,冷却,分离提纯得到粗产品.

回答下列问题:
(1)上述生成FeCl2的反应中,还原剂是C6H5Cl.
(2)实验装置中,仪器B的作用是防止安全瓶内的水分进入A装置,导致FeCl2变质,虚线框内应选择的安全瓶(盛有蒸馏水)是c.(填标号)
(3)实验过程中控制反应温度接近或超过C6H5Cl的沸点,C6H5Cl不会有明显损失,原因是_实验使用了冷凝回流装置.
(4)冷却反应后的实验装置,对三颈烧瓶内的物质进行过滤、洗涤、干燥,得到粗产品.
①洗涤沉淀所用的试剂应为b.(填标号)
a.蒸馏水 b.苯 c.烧碱溶液
②回收滤液中C6H5Cl的方案为蒸馏滤液,并收集132℃馏分.
(5)用x mol•L-1NaOH溶液滴定安全瓶中得到的盐酸,消耗少y mLNaOH溶液,则反应中氯化铁的转化率为$\frac{x•y×1{0}^{-3}×2×162.5}{a}×100%$(只列出计算式).
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38此温度下在实验室中配制100mL5.0mol•L-1,FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入2mol•L-1的盐酸2.5mL(总体积忽略加入盐酸体积).
1.下列关于有机化合物的认识正确的是( )
| A. | 苯中加入溴水后溴水层颜色变浅,这是由于发生了取代反应 | |
| B. | 乙烯和苯分子中所有原子在同一平面上 | |
| C. | 一氯丙烷(C3H7Cl)的同分异构体共有3种 | |
| D. | 标准状况下,2.24LCHCl3含有的分子数为0.1NA |
16.以下实验操作及现象合理的是( )
| A. | 为检验SO42-需要滴加稀硝酸酸化的BaCl2溶液并观察是否有白色沉淀生成 | |
| B. | 把光洁无锈的铁丝放在煤气灯外焰灼烧至与原来的火焰颜色相同时,蘸取K2CO3溶液并灼烧,透过蓝色钴玻璃可观察到火焰为淡紫色 | |
| C. | 向盛有足量苯酚溶液的试管中滴加少量稀溴水,可观察到白色沉淀生成 | |
| D. | 实验室制备乙炔时,常用NaOH溶液除去产生的H2S、PH3等杂质 |