题目内容
(2010?海淀区二模)已知:H2(g)+
O2(g)=H2O(l)△H=-285.8kJ?mol-1;CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ?mol-1
现有H2和CH4的混合气体112L(标准状况),使其完全燃烧生成CO2(g)和H2O(l),共放出热量3242.5kJ,则原混合气体中H2和CH4的物质的量之比是( )
| 1 |
| 2 |
现有H2和CH4的混合气体112L(标准状况),使其完全燃烧生成CO2(g)和H2O(l),共放出热量3242.5kJ,则原混合气体中H2和CH4的物质的量之比是( )
分析:H2和CH4的混合气体112L(标准状况)物质的量为5mol,计算混合物的平均燃烧热为
kJ/mol=648.5kJ/mol,根据十字交叉法计算原混合气体中H2和CH4的物质的量之比.
| 3242.5 |
| 5 |
解答:解:H2和CH4的混合气体112L(标准状况)物质的量为
=5mol,
所以混合气体的平均燃烧热为为
kJ/mol=648.5kJ/mol,
由H2(g)+
O2(g)=H2O(1)△H=-285.8kJ?mol-1可知,氢气的燃烧热为285.8kJ/mol;
由CH4(g)+2O2(g)=CO2(g)+2H2O(1)△H=-890.3kJ?mol-1可知,甲烷的燃烧热为890.3kJ/mol.
根据十字交叉法计算原混合气体中H2和CH4的物质的量之比:
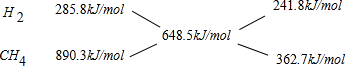
所以原混合气体中H2和CH4的物质的量之比为241.8kJ/mol:362.7kJ/mol=2:3.
故选:D.
| 112L |
| 22.4L/mol |
所以混合气体的平均燃烧热为为
| 3242.5 |
| 5 |
由H2(g)+
| 1 |
| 2 |
由CH4(g)+2O2(g)=CO2(g)+2H2O(1)△H=-890.3kJ?mol-1可知,甲烷的燃烧热为890.3kJ/mol.
根据十字交叉法计算原混合气体中H2和CH4的物质的量之比:

所以原混合气体中H2和CH4的物质的量之比为241.8kJ/mol:362.7kJ/mol=2:3.
故选:D.
点评:考查热化学方程式的意义与计算,难度中等,可以利用混合物的物质的量与放出的热量列放出计算,但计算量较大,计算容易出错,不如十字交叉法简单.根据情况选择方法.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
 (2010?海淀区二模)石墨烯是碳原子构成的单层二维蜂窝状晶格结构(如图所示)的一种碳质新材料,是构建富勒烯、纳米碳管的基本单元,有广泛的用途.下列说法正确的是( )
(2010?海淀区二模)石墨烯是碳原子构成的单层二维蜂窝状晶格结构(如图所示)的一种碳质新材料,是构建富勒烯、纳米碳管的基本单元,有广泛的用途.下列说法正确的是( )