题目内容
(14 分)在T1℃时,向容积为2 L 的密闭容器甲中加人1mol N1、3mol H2及少量固体催 化剂,发生反应N2(g) + 3H2(g) ![]() 2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
(1) 该反应在0 ~l0min 时间内H2的平均反应速率为______,N2的转化率为______。
 (2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
(2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
a.大于25% b.等于25% c.小于25%
(3)右图是在T1℃时密闭容器甲中H2的体积分数随时间t的变化曲线,请在该图中补画出该反应在T2℃(T1 >T2)时H2的体积分数随时间t的变化曲线。
(4)若保持T1℃,在体积也为2 L 的密闭容器乙中通入一定量的N2、H2、NH3,欲使平衡时容器乙中各物质的物质的量与容器甲中完全相同,且起始时反应向正反应方向进行,则通入H2的物质的量x的取值范围是____________。
⑴0.06mol·L-1·min-1 (2分) 40% (3分) ⑵ c (3分)
⑶ 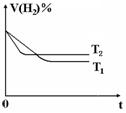 (3分) ⑷ 1.8mol< x <3mol (3分)
(3分) ⑷ 1.8mol< x <3mol (3分)
解析:
(1)设达平衡时,体系内生成2x mol NH3,则有:![]() ,解得x=0.4mol,△c(H2)=0.6mol·L-1,△t=10min,故v(H2)=0.06mol·L-1 ·min-1。N2的转化率=
,解得x=0.4mol,△c(H2)=0.6mol·L-1,△t=10min,故v(H2)=0.06mol·L-1 ·min-1。N2的转化率=![]() =40%。
=40%。
(2)加入0.5mol N2、1.5mol H2、0.5mol NH3相当于加入0.75mol N2、2.25mol H2,与原平衡相比,N2、H2浓度都小于原平衡,所以降低浓度导致反应物的转化率降低,达平衡时体系内NH3的体积分数小于25%。
(3)因T2>T1,所以在T2温度下反应速率更快,达平衡时间更短,但达平衡时H2的体积分数比T1时高,据此可画出对应变化曲线。
(4)甲容器中达平衡时n(H2)=1.8mol,所以x至少应大于1.8mol,要使大平衡时N2、H2、NH3浓度与甲平衡相同,则x<3mol,故有:1.8mol<x<3mol。

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案(每空2分,共14分)在锌与盐酸反应的实验中,某同学得到的结果如下表所示:
| | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于水的时间/s |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | t1 |
| E | 2 | 颗粒 | 15 | t2 |
| F | 2 | 粉末 | 15 | t3 |
| G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
(2)利用所画的曲线图,关于温度影响反应速率的结论是 。
(3)t1 (填“>”或“<”)t4,原因是 。t2 t3(填“>”或“<”),原因是 。
 HCl+HClO,写出该反应化学平衡常数的表达式
HCl+HClO,写出该反应化学平衡常数的表达式 


 2SO3(g)
△H = -196.6 KJ·mol- 1,
2SO3(g)
△H = -196.6 KJ·mol- 1, 与时间t的关系如图2所示,若不改变SO2 (g)和O 2 (g)的量,则:
与时间t的关系如图2所示,若不改变SO2 (g)和O 2 (g)的量,则:
 2C0(g) △H>O,K1
①
2C0(g) △H>O,K1
①

