题目内容
有四组物质,请按要求回答下列问题
(1)同组物质中,X、Y、Z、均是属于电解质的是 (填数字符号).
(2)同组物质中,Y既能与X发生氧化还原反应,又能与Z发生氧化反应反应的是 (填数字符号).
(3)写出第①组X与Y反应的离子方程式 .
(4)若只用一种试剂即可将第②组物质区分开来,该试剂是 .
(5)第③组固体Y中混入了少量的Z,除去少量的Z的最好方法是 .
| X | Y | Z | |
| ① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
| ② | MgCl2溶液 | 酚酞溶液 | NaCl溶液 |
| ③ | Na2O | Na2CO3 | NaHCO3 |
| ④ | KOH溶液 | Al | 稀盐酸 |
(2)同组物质中,Y既能与X发生氧化还原反应,又能与Z发生氧化反应反应的是
(3)写出第①组X与Y反应的离子方程式
(4)若只用一种试剂即可将第②组物质区分开来,该试剂是
(5)第③组固体Y中混入了少量的Z,除去少量的Z的最好方法是
考点:电解质与非电解质,氧化还原反应,物质的分离、提纯和除杂
专题:
分析:(1)电解质为在水溶液中或熔融状态下能够导电的化合物,单质与混合物既不是电解质也不是非电解质,据此解答;
(2)在所给的物质中,Al既能与酸发生氧化还原反应又能与碱发生氧化还原反应;
(3)氢氧化铝与氢氧化钠反应生成偏铝酸钠,据此书写离子反应方程式即可;
(4)氢氧化钠与氯化镁反应生成白色沉淀,遇酚酞变红,与氯化钠不反应,据此解答即可;
(5)碳酸氢钠加热分解生成碳酸钠,据此解答即可.
(2)在所给的物质中,Al既能与酸发生氧化还原反应又能与碱发生氧化还原反应;
(3)氢氧化铝与氢氧化钠反应生成偏铝酸钠,据此书写离子反应方程式即可;
(4)氢氧化钠与氯化镁反应生成白色沉淀,遇酚酞变红,与氯化钠不反应,据此解答即可;
(5)碳酸氢钠加热分解生成碳酸钠,据此解答即可.
解答:
解:(1)电解质为在水溶液中或熔融状态下能够导电的化合物,单质与混合物既不是电解质也不是非电解质,①中氢氧化钠溶液和稀硫酸均为混合物,既不是电解质也不是非电解质;
②中均是溶液,均不是电解质;
③中氧化钠为金属氧化物,属于电解质,后两者均为盐,属于电解质;
④Al是单质,另外两种均是混合物,既不是电解质也不是得电解质,故选③;
(2)在所给的物质中,Al既能与酸发生氧化还原反应又能与碱发生氧化还原反应,故答案为:④;
(3)氢氧化铝与氢氧化钠反应生成偏铝酸钠,离子反应方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)氢氧化钠与氯化镁反应生成白色沉淀,遇酚酞变红,与氯化钠不反应,故答案为:NaOH;
(5)碳酸氢钠加热分解生成碳酸钠,故答案为:加热.
②中均是溶液,均不是电解质;
③中氧化钠为金属氧化物,属于电解质,后两者均为盐,属于电解质;
④Al是单质,另外两种均是混合物,既不是电解质也不是得电解质,故选③;
(2)在所给的物质中,Al既能与酸发生氧化还原反应又能与碱发生氧化还原反应,故答案为:④;
(3)氢氧化铝与氢氧化钠反应生成偏铝酸钠,离子反应方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)氢氧化钠与氯化镁反应生成白色沉淀,遇酚酞变红,与氯化钠不反应,故答案为:NaOH;
(5)碳酸氢钠加热分解生成碳酸钠,故答案为:加热.
点评:本题考查了电解质的判断、离子方程式的书写,题目难度中等,注意掌握电解质与非电解质的概念及判断方法,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
某溶液中含有NH4+、Mg2+、Fe2+、Al3+、SO42-、NO3-六种离子,若向其中加入过量的氢氧化钡溶液,微热并搅拌,再加入过量的氢碘酸,充分反应后溶液中大量减少的离子有( )
| A、NH4+、Fe2+、SO42- |
| B、NH4+、SO42-、NO3- |
| C、Mg2+、Fe2+、SO42- |
| D、Fe2+、Al3+、SO42- |
下列关于胶体的叙述,正确的是( )
| A、胶体区别于其他分散系的本质特征是胶体分散质的微粒直径在10-9~10-7 m之间 | ||||
B、制备氢氧化铁胶体的化学方程式是FeCl3+3H2O
| ||||
| C、用平行光照射NaCl溶液和Fe(OH)3胶体时,产生相同的现象 | ||||
| D、Fe(OH)3胶体能使水中悬浮的固体颗粒沉降,以达到净水的目的,此无菌净水可直接饮用 |
设NA表示阿伏加德罗常数,下列叙述中不正确的是( )
| A、同温同压下,相同体积的氢气和氦气具有的原子数均为NA |
| B、1.7g的OH-中含有的电子数为NA |
| C、常温常压下,48gO3含有的氧原子数为3NA |
| D、11.2g 铁粉与5.6L氯气(标准状况下)充分反应后,反应中转移的电子数为0.5 NA |
下列有关实验的叙述正确的是( )
| A、蒸干AlCl3溶液可得纯净的无水氯化铝 |
| B、用碱式滴定管量取20.00mL酸性高锰酸钾溶液 |
| C、用pH试纸测定溶液的pH时预先要用蒸馏水湿润 |
| D、实验室配制SnCl2 溶液时,需要加入少量的盐酸 |

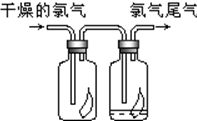 (1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式
(1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式