题目内容
9.下列说法正确的是( )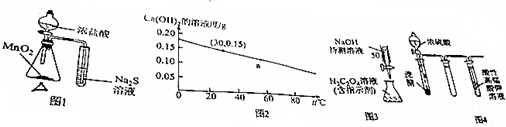
| A. | 图1的装置可用于比较MnO2、Cl2、S的氧化性 | |
| B. | 图2可知:30℃时Ca(OH)2溶液的浓度一定大于60℃时的温度 | |
| C. | 图3的装置可用于已知浓度的H2C2O4溶液测定未知浓度的NaOH溶液 | |
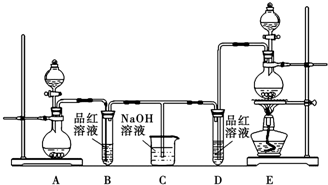
| D. | 图4的实验现象:酸性高锰酸钾溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去 |
分析 A.同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
B.根据图知,30℃时Ca(OH)2溶液的溶解度一定大于60℃时的温度,但30℃时Ca(OH)2溶液的浓度不一定大于60℃时的温度;
C.酸式滴定管只能盛放酸性溶液,碱性溶液应该用碱式滴定管盛放;
D.乙醇被高锰酸钾溶液氧化生成乙酸.
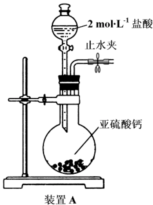
解答 解:A.该实验中,加热条件下,浓盐酸和二氧化锰反应生成氯气,氯气具有强氧化性,能氧化硫化钠生成硫单质,浓盐酸和二氧化锰的反应中二氧化锰是氧化剂、氯气是氧化物,所以氧化性:二氧化锰大于氯气;氯气和硫化钠的反应中,氯气是氧化剂、S是氧化产物,则氧化性氯气大于S,由此得出氧化性MnO2>Cl2>S,故A正确;
B.根据图知,30℃时Ca(OH)2溶液的溶解度一定大于60℃时的温度,但30℃时Ca(OH)2溶液的浓度不一定大于60℃时的温度,可能相等也可能小于,故B错误;
C.酸式滴定管只能盛放酸性溶液,碱性溶液应该用碱式滴定管盛放,NaOH溶液应该用碱式滴定管盛放,故C错误;
D.乙醇能被高锰酸钾溶液氧化生成乙酸而使酸性高锰酸钾溶液褪色,所以酸性高锰酸钾溶液褪色但没有气体生成,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及氧化性强弱比较、溶解度与浓度关系、仪器的选取、乙醇的性质等知识点,侧重考查学生分析判断及基本操作能力,明确实验原理及基本操作方法是解本题关键,注意从实验操作规范性及评价性分析解答,易错选项是BD.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
19.某温度时,N2与H2反应过程中的能量变化如图所示.下列叙述正确的是( )
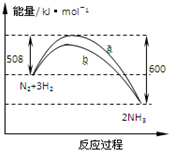

| A. | 1 mo N2与3 mo H2反应可以放出92 kJ的热量 | |
| B. | b曲线是加入催化剂时的能量变化曲线 | |
| C. | 加入催化剂,该反应的焓变减小 | |
| D. | 正反应的活化能等于逆反应的活化能 |
20.下列叙述正确的是( )
| A. | 1molCO2的质量为44g/mol | |
| B. | CO2的摩尔质量为44g | |
| C. | CO2的摩尔质量等于CO2的相对分子质量 | |
| D. | NA个CO2的质量与CO2的相对分子质量在数值上相同(NA为阿伏加德罗常数) |
17.金属钠着火后,可用来灭火的是( )
| A. | 水 | B. | 煤油 | C. | 沙子 | D. | 泡沫灭火器 |
14.向一定浓度的Na2Si03溶液里通入过量CO2气体,发生化学反应,得到无色、透明的液体,该液体能发生丁达尔效应.下列叙述正确的是( )
| A. | 发生的化学反应是复分解反应 | |
| B. | 反应的生成物中有Na2CO3 | |
| C. | 反应后形成的混合物的聚集颗粒直径为1~100nm | |
| D. | 反应说明硅酸易溶于水 |
2.能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛地开发和应用前景.反应:
CO(g)+2H2(g)?CH3OH(g)
①下表所列数据是反应在不同温度下的化学平衡常数(K).
由表中数据判断△H1<0(选填“>”“=”或“<”),根据该反应特点,此反应自发进行的条件是低温(选填“高温”“低温”或“任何温度”)
②某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.2mol•L-1,则CO的转化率为80%.
CO(g)+2H2(g)?CH3OH(g)
①下表所列数据是反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.2mol•L-1,则CO的转化率为80%.
 ,B
,B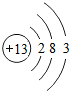 ,二者离子半径:Na+>Al3+(填离子符号).
,二者离子半径:Na+>Al3+(填离子符号).