题目内容
【题目】已知下列反应的热化学方程式为: C(s)+O2(g)=CO2(g)△H1=﹣393.5kJ/mol
CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H2=﹣870.3kJ/mol
H2(g)+ ![]() O2(g)=H2O(l)△H3=﹣285.8kJ/mol
O2(g)=H2O(l)△H3=﹣285.8kJ/mol
2C(s)+2H2(g)+O2(g)=CH3COOH(l) 的反应热△H(焓变)为( )
A.488.3 kJ/mol
B.﹣488.3 kJ/mol
C.﹣244.15 kJ/mol
D.244.15 kJ/mol
【答案】B
【解析】解:已知:(1)C(s)+O2(g)═CO2(g)△H2=﹣393.5kJmol﹣1(2)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=﹣870.3kJmol﹣1(3)H2(g)+ ![]() O2(g)═H2O(l)△H3=﹣285.8kJmol﹣1据盖斯定律将(2)×2+(3)×2﹣(1)可得:2C(s)+2H2(g)+O2(g)═CH3COOH(l)△H=(﹣393.5kJmol﹣1)×2+(﹣285.8kJmol﹣1)×2﹣(﹣870.3kJmol﹣1)=﹣488.3kJ/mol, 故选B.
O2(g)═H2O(l)△H3=﹣285.8kJmol﹣1据盖斯定律将(2)×2+(3)×2﹣(1)可得:2C(s)+2H2(g)+O2(g)═CH3COOH(l)△H=(﹣393.5kJmol﹣1)×2+(﹣285.8kJmol﹣1)×2﹣(﹣870.3kJmol﹣1)=﹣488.3kJ/mol, 故选B.

 阅读快车系列答案
阅读快车系列答案【题目】炼油厂常将裂解产生的其它烯烃加氢,对产物再次裂解以提高乙烯产量.相关加成反应如下: ①  (g)+H2(g)CH3CH2CH2CH3(g)△H1
(g)+H2(g)CH3CH2CH2CH3(g)△H1
②  (g)+H2(g)CH3CH2CH2CH3(g)△H2
(g)+H2(g)CH3CH2CH2CH3(g)△H2
(1)已知反应①、反应②平衡常数k1、k2如下,下列叙述正确的是;
温度(℃) | 300 | 320 | 340 |
K1 | 4.8×10﹣4 | 2.5×10﹣4 | 1.3×10﹣4 |
K2 | 8.4×105 | 3.5×103 | 1.6×103 |
A.△H1>0;△H2<0
B.反应①、反应②都是丙烯加氢,所以△H1═△H2
C.相同条件下反应②的转化率大于反应①的转化率
D.从平衡常数推测,相同条件下反应②的反应速率很大,反应①的反应速率很小
(2)2﹣丁烯的顺、反异构转换过程的△H═(用△H1、△H2表示)  (g)→
(g)→  (g)△H
(g)△H
(3)在一定温度下,将等物质的量的反式2﹣丁烯和H2充入2L密闭容器中,发生反应②,容器内各物质浓度如图所示: 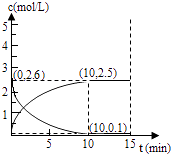
①前10分钟,平均反应速率v(H2)为molL﹣1min﹣1
②该温度下,此反应平衡常数K=(平衡常数不用写单位)
(4)已知表示H2和CH3CH2CH3标准燃烧热的热化学方程式为: H2(g)+ ![]() O2(g)→H2O(l)△H═﹣285.8kJmol﹣1
O2(g)→H2O(l)△H═﹣285.8kJmol﹣1
CH3CH2CH3(g)+5O2(g)→3CO2(g)+4H2O(l)△H═﹣2215kJmol﹣1
丁烯加成反应的热化学方程式为:
CH3CH=CH2(g)+H2(g)→CH3CH2CH3(g)△H═﹣125.4kJmol﹣1
则表示CH3CH=CH2标准燃烧热的热化学方程式为 .