题目内容
一块钠变质为1.55g钠、氧化钠、过氧化钠的混合物,将此混合物用足量的水溶解后,产生标况下气体336mL,在所得溶液中加入60mL、1mol/L的盐酸,恰呈中性.则原钠块的质量为( )
| A、0.92g |
| B、1.15g |
| C、1.27g |
| D、1.38g |
考点:化学方程式的有关计算,钠的化学性质
专题:几种重要的金属及其化合物
分析:钠、氧化钠、过氧化钠的混合物与水反应生成NaOH溶液,在所得溶液中加入60mL、1mol/L的盐酸,恰呈中性,溶质为NaCl,则n(Na+)=n(Cl-),据此计算出钠离子的物质的量,再根据质量守恒计算出原钠块的物质的量及质量.
解答:
解:钠、氧化钠、过氧化钠的混合物,与水反应生成溶质为NaOH,然后用盐酸滴定至中性,此时最终溶质为NaCl,则溶液中:n(Na+)=n(Cl-),
50mL、1mol/L的盐酸中含有氯离子的物质的量为:n(Cl-)=n(HCl)=1mol/L×0.06L=0.06mol,
则n(Na+)=n(Cl-)=0.06mol,
根据质量守恒,原钠块的质量为:m(Na)=23g/mol×0.06mol=1.38g,
故选D.
50mL、1mol/L的盐酸中含有氯离子的物质的量为:n(Cl-)=n(HCl)=1mol/L×0.06L=0.06mol,
则n(Na+)=n(Cl-)=0.06mol,
根据质量守恒,原钠块的质量为:m(Na)=23g/mol×0.06mol=1.38g,
故选D.
点评:本题考查混合物有关计算、利用方程式计算,题目难度中等,过程繁琐、容易出错,可以利用质量守恒简化计算过程,要求学生具有一定的分析和解决问题的能力.

练习册系列答案
相关题目
设NA为阿伏加德罗常数,下列说法中,正确的是( )
| A、2.4 g金属镁所含电子数目为0.2 NA |
| B、16 g CH4所含原子数目为NA |
| C、17 g NH3 所含氢原子数目为4 NA |
| D、18 g水所含分子数目为NA |
下列关于各物质的化学用语表达正确的是( )
A、四氯化碳的电子式: |
B、丙烷分子的比例模型: |
C、环己烷的结构简式: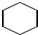 |
| D、乙酸的分子式:CH3COOH |
完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
| A | B | C | D | |
| 实验 | 用CCl4提取溴水中的溴 | 除去乙醇中的I2 | 加热分解MgCl2?6H2O 得到纯净的MgCl2 | 配制100mL0.1000mol/L-1K2CR 2O溶 |
| 装置或仪器 | 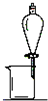 |  | 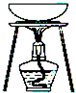 |  |
| A、A | B、B | C、C | D、D |
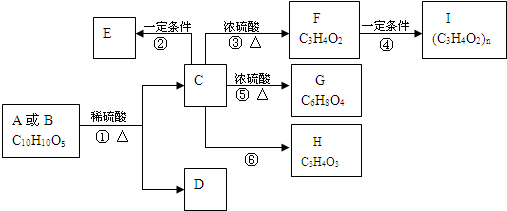
双酚 A是一种重要的化工原料,它的一种合成路线如图所示:
A是一种重要的化工原料,它的一种合成路线如图所示:
下列说法正确的是( )
 A是一种重要的化工原料,它的一种合成路线如图所示:
A是一种重要的化工原料,它的一种合成路线如图所示:下列说法正确的是( )

| A、1mol双酚A最多可与2mol Br2反应 |
| B、G物质是乙醛的同系物 |
| C、E物质的名称是1-溴丙烷 |
D、反应③的化学方程式是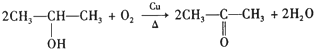 |
下列实验中所选用的仪器或操作合理的是( )
| A、用紫色石蕊试液作指示剂测定NaOH溶液的物质的量浓度 |
| B、用湿润pH试纸测定某H2SO4溶液的pH |
| C、用酸式滴定管量取25.00 mL高锰酸钾溶液 |
| D、中和滴定实验时,用待测液润洗锥形瓶 |