题目内容
10.将30mL0.5mol•L-1NaOH溶液加水稀释到500mL,NA表示阿伏伽德罗常数的值,关于稀释后溶液的叙述不正确的是( )| A. | 溶液中OH-浓度为0.03mol•L-1 | |
| B. | 该溶液中含Na+个数为0.015NA | |
| C. | 向原溶液中加入470mL蒸馏水即可 | |
| D. | 该溶液中含有氧原子个数大于0.015NA |
分析 A.稀释过程中溶质的物质的量不变,据此计算出稀释后溶液中氢氧根离子浓度;
B.稀释过程中钠离子数目不变,根据n=cV计算出稀释后溶液中钠离子的物质的量及数目;
C.氢氧化钠溶液和水的密度不同,计算溶液体积时不能简单加和;
D.溶液中溶剂水分子中也含有氧原子.
解答 解:30mL0.5mol•L-1NaOH溶液中含有氢氧化钠的物质的量为:0.5mol/L×0.03L=0.015mol,
A.稀释过程中氢氧化钠的物质的量不变,则稀释后溶液中氢氧根离子的浓度为:$\frac{0.015mol}{0.5L}$=0.03mol/L,故A正确;
B.稀释过程中钠离子的数目不变,则稀释后溶液中钠离子的物质的量为0.015mol,含Na+个数为0.015NA,故B正确;
C.原氢氧化钠溶液密度与水的密度不同,则加入水的体积不是470mL,应该用500ml的容量瓶配制,故C错误;
D.稀释后溶液中含有0.015mol氢氧化钠,溶质中含有氧原子的物质的量为0.015mol,由于水中含有氧原子,则该溶液中含有氧原子个数大于0.015NA,故D正确;
故选C.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式为解答关键,注意掌握物质的量与物质的量浓度、阿伏伽德罗常数之间的关系,D为易错点,注意水分子中也含有氧原子.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案
相关题目
20.不属于氮的固定的变化是( )
| A. | 豆科植物的根瘤菌把空气中的氮气转化为氨 | |
| B. | 氮气和氢气在适宜条件下合成氨 | |
| C. | 氮气和氧气在放电条件下生成NO | |
| D. | 工业上用氨和二氧化碳合成尿素 |
18.下列叙述不正确的是( )
| A. | CO2的摩尔质量是44g•mol-1,表示1molCO2的质量为44g | |
| B. | 硫酸溶液物质的量的浓度为1mol•L-1表示1L溶液中含有1mol硫酸 | |
| C. | 气体摩尔体积Vm≈22.4mol•L-1,表示1mol任何气体的体积都约为22.4L | |
| D. | 阿伏加德罗常数NA≈6.02×1023mol-1,表示1mol任何粒子集合体所含的粒子数约为6.02×1023 |
5.3.04g铜镁合金完全溶解于100mL14.0mol•L-1的浓硝酸中,得到NO2和N2O4的混合气体2240mL(标准状况),向反应后的溶液中加入2.0mol•L-1NaOH溶液,当金属离子完全沉淀时,得到5.08g沉淀.下列说法不正确的是( )
| A. | 该合金中铜与镁的物质的量之比是2:1 | |
| B. | 被还原的硝酸的物质的量是0.12mol | |
| C. | 得到5.08g沉淀时,加入NaOH溶液的体积是700mL | |
| D. | NO2和N2O4的混合气体中,NO2的体积分数是80% |
5.分子式为C4H1Cl9的同分异构体共有(不考虑立体异构)( )
| A. | 4种 | B. | 7种 | C. | 9种 | D. | 10种 |

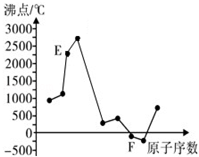 A、B、C、D、E、F是元素周期表中前20号元素,它们的原子序数依次增大.A、B可分别与C组成常见化合物AC、AC2、BC、BC2;D元素的焰色反应呈黄色;E、F两元素单质的沸点与元素原子序数的关系如图(图中原子序数连续).
A、B、C、D、E、F是元素周期表中前20号元素,它们的原子序数依次增大.A、B可分别与C组成常见化合物AC、AC2、BC、BC2;D元素的焰色反应呈黄色;E、F两元素单质的沸点与元素原子序数的关系如图(图中原子序数连续).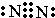 ,化合物AC2的结构式O=C=O;C、D、F对应的简单离子半径由小到大的顺序为Na+<O2-<Cl-(用离子符号表示).
,化合物AC2的结构式O=C=O;C、D、F对应的简单离子半径由小到大的顺序为Na+<O2-<Cl-(用离子符号表示).