题目内容
已知:2Fe2++Br2=2Fe3++2Br-;Cl2+2Br-=Br2+2Cl-;在含n mol FeBr2的溶液中,通入Cl2,有x mol Cl2发生反应.
(1)当x≤
时,反应的离子方程式为
(2)当反应的离子方程式为:3Cl2+2Fe2++4Br-=2Br2+2Fe3++6Cl- 时,x与n的关系为
(3)当Fe2+和Br-同时被氧化时,x与n的关系是
(4)当x=n时,反应后氧化产物的物质的量为 .
(1)当x≤
| n |
| 2 |
(2)当反应的离子方程式为:3Cl2+2Fe2++4Br-=2Br2+2Fe3++6Cl- 时,x与n的关系为
(3)当Fe2+和Br-同时被氧化时,x与n的关系是
(4)当x=n时,反应后氧化产物的物质的量为
考点:氧化还原反应的计算
专题:
分析:还原能力强弱顺序为Fe2+>Br-,则逐滴滴入氯水,则先后发生:Cl2+2Fe2+=2Fe3++2Cl-、Cl2+2Br-=2Cl-+Br2,结合对应物质的物质的量判断反应的程度,并结合反应的离子方程式计算.
解答:
解:还原能力强弱顺序为Fe2+>Br-,则逐滴滴入氯水,则先后发生:Cl2+2Fe2+=2Fe3++2Cl-、Cl2+2Br-=2Cl-+Br2,
(1)当x≤
时,氯气不足,只发生Cl2+2Fe2+=2Fe3++2Cl-,故答案为:Cl2+2Fe2+=2Fe3++2Cl-;
(2)当反应的离子方程式为:3Cl2+2Fe2++4Br-=2Br2+2Fe3++6Cl- 时,FeBr2全部被氧化,由离子方程式可知,则氯气应足量,如FeBr2为1mol,则氯气至少为1.5mol,则应满足x≥
,故答案为:x≥
;
(3)当x=
时,只氧化Fe2+,当大于
时,可氧化Br-,则x>
时,Fe2+和Br-同时被氧化,故答案为:x>
;
(4)当x=n时,只氧化Fe2+,先后发生:Cl2+2Fe2+=2Fe3++2Cl-、Cl2+2Br-=2Cl-+Br2,
0.5n n n 0.5n 0.5n
则氧化产物的物质的量为
mol或
mol,
故答案为:
mol或
mol.
(1)当x≤
| n |
| 2 |
(2)当反应的离子方程式为:3Cl2+2Fe2++4Br-=2Br2+2Fe3++6Cl- 时,FeBr2全部被氧化,由离子方程式可知,则氯气应足量,如FeBr2为1mol,则氯气至少为1.5mol,则应满足x≥
| 3n |
| 2 |
| 3n |
| 2 |
(3)当x=
| n |
| 2 |
| n |
| 2 |
| n |
| 2 |
| n |
| 2 |
(4)当x=n时,只氧化Fe2+,先后发生:Cl2+2Fe2+=2Fe3++2Cl-、Cl2+2Br-=2Cl-+Br2,
0.5n n n 0.5n 0.5n
则氧化产物的物质的量为
| 3n |
| 2 |
| 3x |
| 2 |
故答案为:
| 3n |
| 2 |
| 3x |
| 2 |
点评:本题考查氯气的性质以及方程式的计算,注意根据离子的还原性判断反应的先后顺序,为解答该题的关键,注意结合反应的离子方程式解答该题,难度中等.

练习册系列答案
相关题目
下列图示与对应叙述相符合的是( )
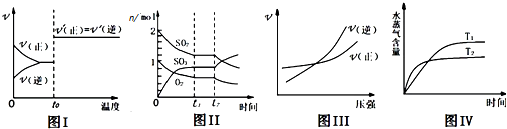

| A、图I:反应CO+NO2═CO2+NO达平衡后,升高温度时反应速率随时间的变化 |
| B、图Ⅱ:反应2SO2+O2═2SO3 达平衡后,缩小容器体积时各成分的物质的量随时间的变化 |
| C、图Ⅲ:反应N2+3H2═2NH3在恒温情况下,反应速率与压强的关系 |
| D、图Ⅳ:反应CO2(g)+H2(g)═CO(g)+H2O(g)△H>0,水蒸气含量随时间的变化 |
如图是10mL量筒的一部分,数字XY之间相差2mL若X=6,则量筒所盛液体的体积是( )
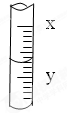

| A、4.30mL |
| B、4.6mL |
| C、4.3mL |
| D、4.60mL |
已知反应X+Y=M+N为放热反应,对该反应的下列说法中正确的( )
| A、X的能量一定高于M |
| B、因该反应为放热反应,故不必加热就可发生 |
| C、Y的能量一定高于N |
| D、X和Y的总能量一定高于M和N的总能量 |
下列说法中错误的是( )
| A、同一原子中一定没有能量相同的电子 |
| B、6C的电子排布式1s22s22px2违反了洪特规则 |
| C、电子排布式1s22s22p63s23p63d3违反了能量最低原理 |
| D、电子排布式1s22s22p63s23p10违反了泡利原理 |
下列指定反应的离子方程式正确的是( )
| A、向苯酚钠溶液中通入少量的CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- | ||||
| B、FeS固体放入稀硝酸溶液中:FeS+2H+=Fe2++H2S↑ | ||||
| C、(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ | ||||
D、用惰性电极电解氯化钠溶液:2Cl-+2H+
|
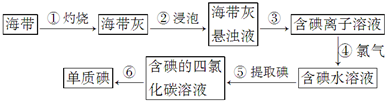
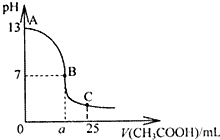 (1)用已知浓度的NaOH溶液测定某H2SO4溶液的浓度.选择
(1)用已知浓度的NaOH溶液测定某H2SO4溶液的浓度.选择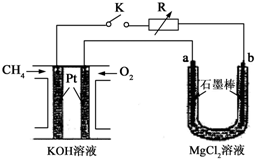 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源进行氯化镁溶液电解实验,电解装置如图所示.
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源进行氯化镁溶液电解实验,电解装置如图所示.