题目内容
某同学按下图所示的装置进行试验。 A、B为两种常见金属,它们的硫酸盐可溶于水。当K闭合时,在交换膜处![]() 从右向左移动。下列分析正确的是
从右向左移动。下列分析正确的是

A.B的电极反应:![]()
B.在ASO4溶液中,(![]() )浓度减小
)浓度减小
C.![]() 电极上有
电极上有![]() 产生,发生还原反
产生,发生还原反
应
D.反应初期,![]() 电极周围出现白色胶状沉淀
电极周围出现白色胶状沉淀
D
解析:
据右面图示可知,左侧装置为原电池,右侧为电解池。由题意在交换膜处![]() 从右向左移动可知,A电极显正电性,即A为原电池的负极,电极反应式为:A-2e-=A2+, A2+的浓度增大,B电极为原电池的正极,电极反应式为:B2++2e-=B,故A、B均错。Y电极与原电池的正极B相连,即y电极为电解池的阳极,发生氧化反应,电极反应式为:2Cl一 一2e一=C12↑。X电极为电解池的阴极,其电极反应式为2H+ + 2e-+ =H2 ↑,由于H+来自于H2O,从而破坏水的电离平衡,使溶液显碱性,所以会发生此反应:AI3++3OH-=Al(OH)3,故D正确。
从右向左移动可知,A电极显正电性,即A为原电池的负极,电极反应式为:A-2e-=A2+, A2+的浓度增大,B电极为原电池的正极,电极反应式为:B2++2e-=B,故A、B均错。Y电极与原电池的正极B相连,即y电极为电解池的阳极,发生氧化反应,电极反应式为:2Cl一 一2e一=C12↑。X电极为电解池的阴极,其电极反应式为2H+ + 2e-+ =H2 ↑,由于H+来自于H2O,从而破坏水的电离平衡,使溶液显碱性,所以会发生此反应:AI3++3OH-=Al(OH)3,故D正确。

 阅读快车系列答案
阅读快车系列答案
| |||||||||||
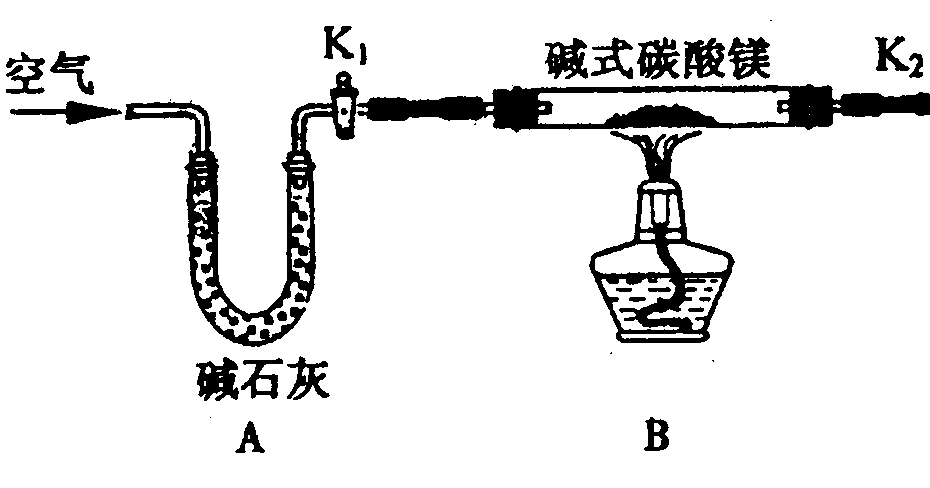
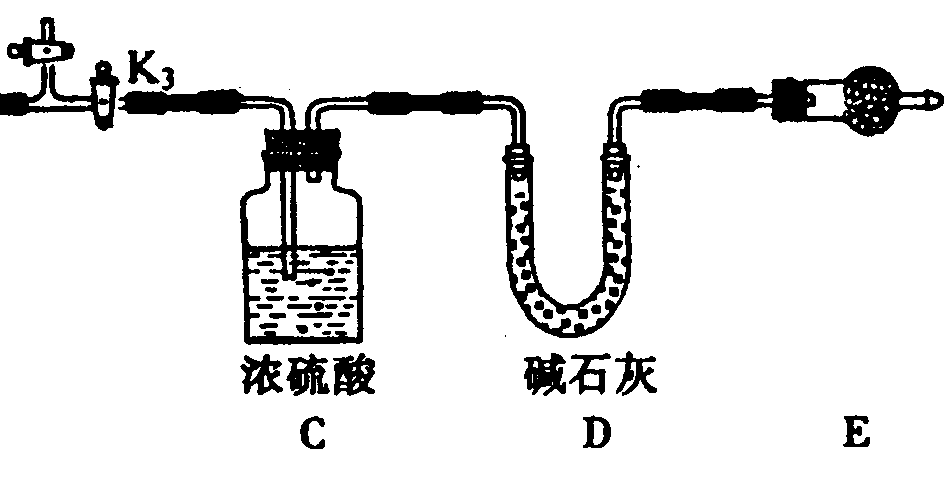
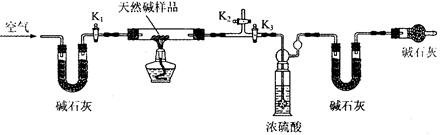

 ,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置
,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置

 ,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置
,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置
