题目内容
欲证明一瓶无色液体是纯水,可靠的实验方法是( )
| A、测得其pH=7 |
| B、电解时得到H2与O2的体积比为2:1 |
| C、遇钠生成氢气 |
| D、1.01×105Pa时沸点为100℃ |
考点:物质的检验和鉴别的基本方法选择及应用
专题:实验题
分析:纯水在常压下的沸点为1000C,可通过测定沸点的方法证明是否为纯水,强酸强碱盐的水溶液pH=7,只要含有水,就能跟钠反应生成氢气,电解活泼金属的含氧酸盐时,得到H2、O2,体积比为2:1,以此解答该题.
解答:
解:A.强酸强碱盐的水溶液pH=7,不能确定是否为纯水,故A错误;
B.电解活泼金属的含氧酸盐时,得到H2、O2,体积比为2:1,不能确定是否含有纯水,故B错误;
C.只要含有水,就能跟钠反应生成氢气,不能确定是否为纯水,故C错误;
D.纯水在常压下的沸点为1000C,可通过测定沸点的方法证明是否为纯水,故D正确.
故选D.
B.电解活泼金属的含氧酸盐时,得到H2、O2,体积比为2:1,不能确定是否含有纯水,故B错误;
C.只要含有水,就能跟钠反应生成氢气,不能确定是否为纯水,故C错误;
D.纯水在常压下的沸点为1000C,可通过测定沸点的方法证明是否为纯水,故D正确.
故选D.
点评:本题考查物质的检验和鉴别,为高频考点,侧重学生的分析、实验能力的考查,题目难度中等,注意盐类的水解和电解原理,AB为易错点.

练习册系列答案
相关题目
关于浓硫酸的叙述正确的是( )
| A、浓硫酸具有吸水性,因而能使蔗糖炭化 |
| B、浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 |
| C、常温下,金属铁遇浓硫酸时会在表面生成致密的氧化膜而发生钝化 |
| D、50mL 18mol?L-1硫酸中加入足量的铜粉反应放出二氧化硫气体少于10.08L |
可用如图所示装置制取、干燥、收集并吸收多余气体的是( )
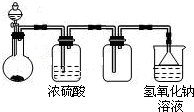

| A、浓氨水与氧化钙固体反应制氨气 |
| B、稀硫酸与硫化亚铁固体反应制硫化氢 |
| C、浓盐酸与次氯酸钙固体反应制氯气 |
| D、饱和食盐水与电石反应制乙炔 |
下列除质或鉴别方法可行的是( )
| A、用过量氨水除去Al3+溶液中的少量Fe3+ |
| B、将混合气体通过灼热的铜网除去N2中的少量O2 |
| C、向某溶液中加HCl酸化的BaCl2溶液,产生白色沉淀,则该溶液中一定含有SO42- |
| D、向澄清石灰水中通入少量气体产生沉淀,过量时沉淀溶解,说明该气体一定是CO2 |
设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A、标准状况下,将5.6L的O2和5.6LNO的混合后的分子数约为0.5NA |
| B、2L 0.5mol/L BaCl2溶液中,阳离子所带电荷数为 NA |
| C、常温常压下,将0.2mol铝片投入含0.6molH2SO4的浓硫酸中,生成0.3 NA个SO2分子 |
| D、42g丙烯气体中,含有的σ键数目为8NA |
对于硫酸工业中SO2的催化氧化反应:2SO2+O2
2SO3,下列说法错误的是( )
| 催化剂 |
| 加热 |
| A、使用催化剂是为了加快反应速率 |
| B、增大O2浓度可以使SO2转化率达到100% |
| C、加压可以增大反应速率 |
| D、增大O2浓度可以增大反应速率 |