题目内容
下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4
④结合质子(H+)能力:OH->HCO3->CH3COO-.
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4
④结合质子(H+)能力:OH->HCO3->CH3COO-.
| A、①③ | B、②④ | C、①④ | D、②③ |
考点:非金属在元素周期表中的位置及其性质递变的规律,金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:元素的非金属性越强,对应的氢化物越稳定,对应的最高价氧化物的水合物的酸性越强,对应的阴离子结合质子的能力越弱,同周期元素原子序数越大,原子半径越小,一般来说,不同晶体的熔点:原子晶体>金属晶体>分子晶体,以此解答.
解答:
解:①非金属性F>O>S,元素的非金属性越强,对应的氢化物越稳定,故①错误;
②Na、Mg位于相同周期,同周期元素从左到右原子半径逐渐减小,则原子半径Na>Mg,O位于第二周期,原子半径在三者之间最小,故②正确;
③非金属性Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水合物的酸性越强,故③错误;
④已知酸性H2O<H2CO3<CH3COOH,酸性越强,对应的阴离子结合质子的能力越弱,故④正确.
故选B.
②Na、Mg位于相同周期,同周期元素从左到右原子半径逐渐减小,则原子半径Na>Mg,O位于第二周期,原子半径在三者之间最小,故②正确;
③非金属性Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水合物的酸性越强,故③错误;
④已知酸性H2O<H2CO3<CH3COOH,酸性越强,对应的阴离子结合质子的能力越弱,故④正确.
故选B.
点评:本题考查元素周期表和元素周期律知识,为高频考点,侧重于学生的分析能力的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
等浓度的NaOH溶液与氢硫酸溶液反应,下列说法不正确的是( )
| A、溶液中始终有:c(Na+)+c(H+)═2c(S2-)+c(HS-)+c(OH-) |
| B、t溶液呈中性时:c(Na+)═c(HS-)+c(S2-) |
| C、等体积混合后溶液中一定有:c(H2S)+c(H+)═c(S2-)+c(OH-) |
| D、恰好完全中和后的溶液中:c(Na+)>2c(S2-) |
己知反应A(s)+B(g)?C(g)+D(g)的化学平衡常数和温度的关系如表下列说法正确的是( )
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 化学平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A、该反应的化学平衡常数表达式为:K=
| ||
| B、该反应为吸热反应 | ||
| C、单位时间内生成B和D的物质的量相等时,该反应处于平衡状态 | ||
| D、其它条件不变时,增大体系的压强,化学平衡常数减小 |
下列属于取代反应的是( )
| A、甲烷燃烧 |
| B、在镍催化下,苯与氢气反应生成环己烷 |
| C、光照条件下甲烷与氯气反应生成一氯甲烷 |
| D、乙烯使溴水褪色 |
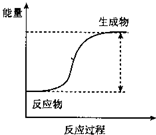 (1)反应的分类研究:从能量变化角度分,将反应分为放热反应和吸热反应.下列反应中能量变化符合如图所示的是
(1)反应的分类研究:从能量变化角度分,将反应分为放热反应和吸热反应.下列反应中能量变化符合如图所示的是