题目内容
镁锌合金粉末7.7g恰好与一定质量20%的稀硫酸完全反应,将反应后的溶液蒸发,经处理后得到不含结晶水的固体22.1g,则反应中生成氢气的质量为( )
| A、0.1g | B、0.2g |
| C、0.3g | D、0.4g |
考点:有关混合物反应的计算
专题:计算题
分析:最终晶体为MgSO4、ZnSO4,根据质量守恒计算m(SO42-),进而计算n(SO42-),而n(H2)=n(H2SO4)=n(SO42-),再根据m=nM计算生成氢气的质量.
解答:
解:最终晶体为MgSO4、ZnSO4,根据质量守恒,则m(SO42-)=22.1g-7.7g=14.4g,则n(SO42-)=
=0.15mol,而n(H2)=n(H2SO4)=n(SO42-)=0.15mol,则生成氢气的质量为0.15mol×2g/mol=0.3g,
故选C.
| 14.4g |
| 96g/mol |
故选C.
点评:本题考查混合物计算,难度不大,侧重考查学生分析思维与解题方法技巧考查,注意利用守恒法解答.

练习册系列答案
相关题目
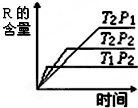 在密闭容器中进行下列反应:M(g)+N(g)R(g)+2L,反应符合右图.下列叙述正确的是( )
在密闭容器中进行下列反应:M(g)+N(g)R(g)+2L,反应符合右图.下列叙述正确的是( )| A、T2>T1,正反应放热,L是液体 |
| B、P2<P1,正反应吸热,L是固体 |
| C、T2<T1,正反应放热,L是气体 |
| D、P2>P1,正反应吸热,L是气体 |
下列行为违背了“环境友好和可持续发展”战略的是( )
| A、对煤进行脱硫、液化、气化加工,提高煤的综合利用率 |
| B、研究以植树秸秆为原料制取生物柴油 |
| C、为加快融雪,在高速路面上大范围使用融雪剂 |
| D、进行以“设计绿色化工工艺,提高原子利用率”为目标的技术革新 |
把2.27gNaHCO3和Na2CO3?10H2O组成的混合物溶于水配成100ml溶液,其中C(Na+)=0.2mol?L-1,若将等质量的该混合物加热至恒重,所得固体质量为( )
| A、0.84g |
| B、1.06g |
| C、1.43g |
| D、2.27g |
在200mL氯化镁和氯化铝的混合液中,Mg2+的物质的量浓度为0.2mol/L,Cl-的物质的量浓度为1.3mol/L.要使Mg2+全部转化为沉淀分离出来,至少需要加入 4mol/L NaOH溶液的体积为( )
| A、40mL | B、72mL |
| C、80mL | D、128mL |
水溶液中能大量共存的一组离子是( )
| A、Ba2+、Na+、Cl-、OH- |
| B、Fe2+、H+、SO42-、NO3- |
| C、Na+、Mg2+、Cl-、CO32- |
| D、K+、Fe3+、NO3-、SCN- |
相对分子质量为72的烷烃,其同分异构体有( )种.
| A、3 | B、4 | C、5 | D、6 |
 探究实验发现,硝酸发生氧化还原反应时,浓度越稀,对应还原产物中氮元素的化合价越低.
探究实验发现,硝酸发生氧化还原反应时,浓度越稀,对应还原产物中氮元素的化合价越低.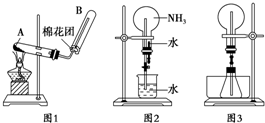 如图1为实验室制取氨的实验装置.
如图1为实验室制取氨的实验装置.