题目内容
15.下列物质属于电解质的是( )| A. | 纯碱 | B. | 浓硫酸 | C. | 氯化钠溶液 | D. | 二氧化硫 |
分析 在水溶液里或融融状态下能导电的化合物是电解质,在水溶液里或熔融状态下都不能导电的化合物是非电解质,无论是电解质还是非电解质都必须是化合物,据此分析.
解答 解:A.纯碱是盐,在水溶液中和熔融状态下均能导电,属于电解质,故A正确;
B.浓硫酸是混合物,既不是电解质也不是非电解质,故B错误;
C.氯化钠溶液是混合物,既不是电解质也不是非电解质,故C错误;
D.二氧化硫本身不能导电,在溶于水时能导电,原因是二氧化硫与水反应生成了亚硫酸,亚硫酸是电解质,故D错误,故选A.
点评 本题考查了电解质和非电解质的概念,难度不大,注意电解质和非电解质的区别.

练习册系列答案
相关题目
6.下列说法错误的是( )
| A. | 卢瑟福提出了带核的原子结构模型 | |
| B. | 已知PM2.5是指大气中直径≤2.5×10-6m的颗粒物,受PM2.5污染的大气不一定能产生丁达尔现象 | |
| C. | 借助仪器来分析化学物质的组成是常用的手段,原子吸收光谱常用来确定物质中含有的非金属元素 | |
| D. | 并不是所有金属元素都可以用焰色反应来确定其存在 |
3.某澄清溶液可能含有以下离子中的若干种:K+、Cl-、NH4+、Mg2+、CO32-、Ba2+、SO42-,现取3份100mL该溶液分别进行如下实验:
试回答下列问题:
(1)根据实验判断混合物中一定存在的离子是K+、NH4+、CO32-、SO42-,无法确定的离子是Cl-.
(2)写出实验2中发生反应的离子方程式NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(3)为了进一步确定可能存在的离子,请设计可行的实验方案:取少量待测液于试管中滴加稀硝酸酸化,再滴加硝酸银溶液,若产生白色沉淀,则说明原溶液中含有Cl-.
| 实验序号 | 实验内容 | 实验结果 |
| 1 | 加AgNO3溶液 | 有白色沉淀生成 |
| 2 | 加足量NaOH溶液并加热 | 收集到气体0.672L (已折算成标准状况下的体积) |
| 3 | 加足量 BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量的稀盐酸,然后干燥、称量 | 第一次称量读数为4.3g, 第二次称量读数为2.33g |
(1)根据实验判断混合物中一定存在的离子是K+、NH4+、CO32-、SO42-,无法确定的离子是Cl-.
(2)写出实验2中发生反应的离子方程式NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(3)为了进一步确定可能存在的离子,请设计可行的实验方案:取少量待测液于试管中滴加稀硝酸酸化,再滴加硝酸银溶液,若产生白色沉淀,则说明原溶液中含有Cl-.
10.下列除去杂质的方法中正确的是( )
| A. | 溴苯中混有溴,加入四氯化碳后,用分液漏斗分液 | |
| B. | 乙醇中混有乙酸,加入NaOH溶液后,用分液漏斗分液 | |
| C. | 乙烷中混有乙烯,加入氢气在一定条件下充分反应 | |
| D. | 苯甲醛中混有苯甲酸,加入生石灰,再加热蒸馏 |
20.将充满20mL NO试管倒置于盛有蒸馏水的烧杯中,然后向试管中通入纯O2,当试管内液面稳定在试管容积的一半时,则通入O2为( )
| A. | 7.5 mL | B. | 17.5 mL | C. | 25.0 mL | D. | 35.0 mL |
7.25℃时,水的电离达到平衡:H2O?H++OH-,△H>0,下列叙述正确的是( )
| A. | 向水中加入固体CH3COONa,平衡正向移动,c(H+)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+) 降低,Kw不变 | |
| C. | 向水中加入少量固体CH3COOH,平衡逆向移动,c(H+)降低 | |
| D. | 将水加热,Kw增大,pH不变 |
4.实验操作的规范是实验的基本要求.下列实验操作正确的是( )
| A. | 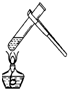 给试管加热 | B. | 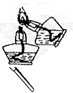 点燃酒精灯 | C. |  滴加液体 | D. | 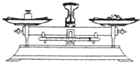 称量10.05g固体 称量10.05g固体 |
5.用惰性电极电解100mL 0.05mol/L的CuSO4的溶液,当电解到阴极刚好有气体析出时,溶液的PH值最接近于(不考虑溶液的体积变化)( )
| A. | 1.0 | B. | 1.3 | C. | 1.7 | D. | 2.0 |
