题目内容
2.下列化学用语正确的是( )| A. | -OH的电子式: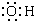 | |
| B. | 硫离子结构示意图: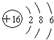 | |
| C. | 氢氧化铜电离方程式:Cu(OH)2═Cu2++2OH- | |
| D. | 乙酸的分子式:C2H4O2 |
分析 A.羟基为中性原子团,氧原子最外层电子数为7;
B.硫离子的最外层满足8电子稳定结构;
C.氢氧化铜为弱碱,电离方程式应该用可逆号;
D.乙酸分子为含有2个C的饱和一元羧酸.
解答 解:A.羟基中含有1个O-H键,为中性原子团,羟基的电子式为 ,故A错误;
,故A错误;
B.硫离子的核电荷数为16,核外电子总数为18,其正确的离子结构示意图为: ,故B错误;
,故B错误;
C.氢氧化铜为弱电解质,电离方程式用可逆号,氢氧化铜正确的电离方程式为:Cu(OH)2?Cu2++2OH-,故C错误;
D.乙酸分子中含有1个甲基和1个羧基,其分子式为:C2H4O2,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、离子结构示意图、电离方程式、分子式等知识,明确常见化学用语的表示方法为解答关键,试题培养了学生的分析能力及规范答题能力.

练习册系列答案
相关题目
12.将盛有12mL NO2和O2的混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积和剩余的2mL气体分别是( )
| A. | 1.2 mL,NO | B. | 2.4 mL,O2 | C. | 3.5 mL,O2 | D. | 4 mL,NO |
13.根据元素周期律及元素周期表的知识分析,下列关系中不正确的是( )
| A. | 酸性强弱:H3PO4>H2SO4>HClO4 | B. | 离子半径大小:F->Na+>Mg2+>Al3+ | ||
| C. | 稳定性大小:SiH4<PH3<H2S<HCl | D. | 碱性强弱:NaOH>Mg(OH)2>Al(OH)3 |
10.化学与生活密切相关,下列说法中不正确的是( )
| A. | Al2O3 熔点高,可用于制作耐高温仪器 | |
| B. | 水果、蔬菜等是碱性食物 | |
| C. | 高纯度的硅单质可用于制作光导纤维 | |
| D. | 绿色化学的核心是从源头上杜绝污染的产生 |
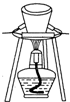
17.下列有关实验原理或操作正确的是( )

| A. | 用湿润的pH试纸测定溶液的pH | |
| B. | 用如图所示装置灼烧碱式碳酸铜[Cu2(OH)2CO3]制取氧化铜 | |
| C. | 用铜丝蘸取草木灰在酒精灯火焰灼烧检验钾元素 | |
| D. | 称取0.4g NaOH,放入100mL容量瓶中,加入蒸馏水溶解,用胶头滴管定容至刻度线,振荡摇匀,配制100mL 0.10mol/L NaOH溶液 |
7.下列鉴别方法不可行的是( )
| A. | 用燃烧法鉴别乙醇、苯和四氯化碳 | |
| B. | 用酸性高锰酸钾溶液鉴别苯、环己烯和环己烷 | |
| C. | 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 | |
| D. | 用水鉴别乙醇、苯和溴苯 |
14.下列实验方案能达到实验目的是( )
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有 乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液, 加热,将反应产生的气体通入溴的四氯化碳溶液 |
| B | 证明HCOOH结构中含有醛 基 | 将1mL 1mol/L HCOOH溶液加入装有银氨溶液 的试管中并水浴加热,观察有无银镜产生 |
| C | 除去甲烷中的乙烯 | 将混合气通入KMnO4溶液中洗气 |
| D | 制取乙烯气体 | 将无水乙醇和浓硫酸混合加热到140℃ |
| A. | A | B. | B | C. | C | D. | D |
11.有关该物质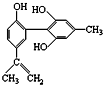 的说法正确的是( )
的说法正确的是( )
 的说法正确的是( )
的说法正确的是( )| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 该分子中的所有碳原子不可能共平面 | |
| C. | 滴入酸性KMnO4溶液,观察紫色褪去,能证明结构中存在碳碳双键 | |
| D. | 1 mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别为4 mol、7 mol |
12.欲除去Cl2中的少量HCl气体,可选用( )
| A. | NaOH溶液 | B. | AgNO3溶液 | C. | 饱和食盐水 | D. | 石灰水 |