题目内容
1.已知:H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ•mol-1.现将一定量的稀盐酸、浓硫酸、稀醋酸分别和1L 1mol•L-1的NaOH溶液恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2和△H3的大小关系为( )| A. | △H1=△H2>△H3 | B. | △H3>△H1>△H2 | C. | △H3>△H2>△H1 | D. | △H2>△H1>△H3 |
分析 H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1;中和热是强酸强碱稀溶液完全反应生成1mol水放出的热量,浓硫酸溶解过程中放热,醋酸是弱电解质存在电离平衡,电离过程是吸热过程,注意放热反应中焓变为负值,据此判断该反应的焓变大小.
解答 解:H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ•mol-1;中和热是强酸强碱稀溶液完全反应生成1mol水放出的热量,
一定量的稀盐酸和1L 1mol•L-1的NaOH溶液恰好完全反应放热57.3kJ;
浓硫酸和1L 1mol•L-1的NaOH溶液恰好完全反应,溶解过程中放热,反应放热大于57.3kJ;
醋酸是弱电解质存在电离平衡,电离过程是吸热程,醋酸和1L 1mol•L-1的NaOH溶液恰好完全反应放热小于57.3kJ;
反应焓变是负值,所以△H3>△H1>△H2,
故选B.
点评 本题考查了反应热与焓变的应用,题目难度不大,注意掌握化学反应与能量变化的关系,明确浓硫酸溶解放热,醋酸电离过程是吸热过程为解答关键.

练习册系列答案
相关题目
13.下列关于1mo1•L-1的BaCl2溶液的叙述中.正确的是( )
| A. | 该溶液中C1-浓度为2mo1•L-1 | |
| B. | 该溶液中Ba2+的物质的量是1mo1 | |
| C. | 可使用250mL容量瓶分两次完成490mL该浓度的BaCl2溶液的配制 | |
| D. | 将208gBaCl2固体溶解在1L水中,形成的溶液的浓度为1mo1•L-1 |
9.下列说法正确的是( )
| A. | 碳-14 核素:148C | |
| B. | HClO 的结构式为 H-O-Cl | |
| C. | 化学反应在物质变化的同时,伴随着能量变化,其表现形式只有吸热和放热两种 | |
| D. | H2S、PH3、HCl、HF 的热稳定性依次增强 |

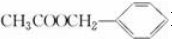 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
 ,B中含氧官能团的名称是羧基.
,B中含氧官能团的名称是羧基.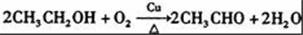 ;
;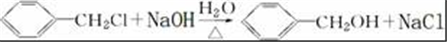 .
.