题目内容
10.元素周期表是学习物质结构与性质的重要工具.如图是元素周期表的一部分,图中所列字母a、b、c、d、e、f、g、m、n、o、r分别代表某一种元素.请回答下列问题.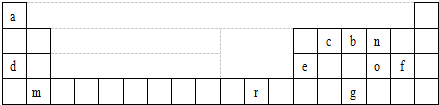
(1)在a~r11种元素有4种金属元素;
(2)m元素在元素周期表中的位置第四周期ⅡA族;
(3)e、n二元素形成的稳定化合物的化学式为Al2O3;
(4)化合物ba3的结构式为
 ;
;(5)用电子式表示化合物d2n的形成过程
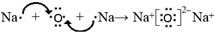 ;
;(6)d的最高价氧化物的水化物与e的最高价氧化物反应的离子方程式2OH-+Al2O3=2AlO2-+H2O.
分析 由元素在周期表的位置可知,a为H,c为C,b为N,n为O,d为Na,e为Al,o为S,f为Cl,m为Ca,r为Cu,g为As,
(1)H、C、N、O、S、Cl、As为非金属,其余为金属;
(2)m为Ca;
(3)e、n二元素形成的稳定化合物为氧化铝;
(4)氨气为三角锥型;
(5)氧化钠为离子化合物;
(6)d的最高价氧化物的水化物为NaOH,e的最高价氧化物为氧化铝,二者反应生成偏铝酸钠和水.
解答 解:由元素在周期表的位置可知,a为H,c为C,b为N,n为O,d为Na,e为Al,o为S,f为Cl,m为Ca,r为Cu,g为As,
(1)在a~r11种,H、C、N、O、S、Cl、As为非金属,共7种非金属元素,Na、Al、Ca、Cu为金属,4种金属元素,故答案为:4;
(2)m为Ca,在周期表的位置为第四周期ⅡA族,故答案为:第四周期ⅡA族;
(3)e、n二元素形成的稳定化合物为氧化铝,化学式为Al2O3,故答案为:Al2O3;
(4)氨气为三角锥型,结构式为 ,故答案为:
,故答案为: ;
;
(5)氧化钠为离子化合物,用电子式表示化合物d2n的形成过程为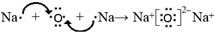 ,故答案为:
,故答案为: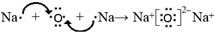 ;
;
(6)d的最高价氧化物的水化物为NaOH,e的最高价氧化物为氧化铝,二者反应生成偏铝酸钠和水,离子反应为2OH-+Al2O3=2AlO2-+H2O,
故答案为:2OH-+Al2O3=2AlO2-+H2O.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、元素周期律、元素化合物为解答的关键,侧重分析与应用能力的考查,注意化学用语的使用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.镁铝合金5.1g加入到100mL 6.0mol•L-1盐酸中,待固体完全溶解后,向溶液中继续逐滴滴入6.0mol•L-1的氢氧化钠溶液,当滴入VmL时沉淀质量达到最大值,继续滴入氢氧化钠至沉淀的量不再变化,将沉淀过滤、洗涤、低温烘干,称重得质量为5.8g.下列说法正确的是( )
| A. | 开始滴入NaOH溶液时立即产生白色沉淀 | |
| B. | 原固体混合物中镁的质量是1.2g | |
| C. | V=100mL | |
| D. | 若将5.1g该合金溶于足量的氢氧化钠溶液,在常温常压下放出3.36L气体 |
18.下列有关叙述正确的是( )
| A. | Cl2、SO2均能使品红溶液褪色,说明二者均有漂白性 | |
| B. | 元素周期表中第IA族全部是金属元素 | |
| C. | 盛有浓硫酸的烧杯敞口放置一段时间后,质量增加 | |
| D. | 硫在纯氧中的燃烧产物是三氧化硫 |
5.要除去下表所列有机物中的杂质(括号内为杂质),从(1)中选择适宜的试剂,从(2)中选择分离提纯的方法,用序号填入表中.
(1)试剂:a.浓硫酸 b.氢氧化钠 c.生石灰 d.碳酸钠 e.水 f.浓溴水
(2)方法:A.过滤 B.分液 C.蒸馏
(1)试剂:a.浓硫酸 b.氢氧化钠 c.生石灰 d.碳酸钠 e.水 f.浓溴水
(2)方法:A.过滤 B.分液 C.蒸馏
| 要提纯的物质 (杂质) | 溴乙烷 (乙醇) | 乙醇 (水) | 乙醇 (乙酸) | 溴苯 (溴) |
| (1)选用试剂 | ||||
| (2)分离方法 |
15.下列物质的电子式错误的是( )
| A. | 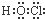 | B. | 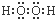 | C. | 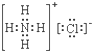 | D. | 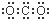 |
19.设NA为阿伏伽德罗常数,下列说法一定正确的是( )
| A. | 4g D2和足量O2反应可生成D2O 2NA个 | |
| B. | 98g H3PO4和H2SO4的混合物中含氢原子2.5NA个 | |
| C. | 6.02×1023个葡萄糖分子约含羟基6NA个 | |
| D. | 1molNa完全燃烧可转移电子NA个 |
12.碘酸钙[Ca(IO3)2]既能补碘又能补钙的新型食品和饲料添加剂.碘酸钙可通过下列途径合成.
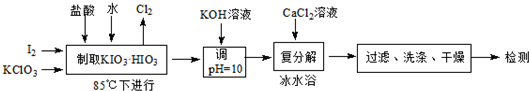
(1)若称取的I2质量为3.810g,为使I2充分氧化,则投料时KClO3的质量至少为3.675;同时生成的氯气体积为336mL(标准状况).
(2)用KOH溶液调节pH的目的是将KIO3•HIO3转变为KIO3.
(3)已知几种盐的溶解度(g/100g水)如下:
碘酸钙的物理性质
复分解时,采用冰水浴的目的是减小Ca(IO3)2在水中的溶解度,使其充分析出;此时所得产品的化学式为Ca(IO3)2•6H2O.
(4)准确称取产品0.6000g于烧标中,加1:1高氯酸20mL,微热溶解后,冷却,配成250.00mL溶液.移取上述溶液50.00mL置于250mL碘量瓶中,加入1:1高氯酸2mL、3gKI(足量)(发生:IO3-+5I-+6H+═3I2+3H2O),盖上瓶盖,暗处放置3min,加50mL水,加入0.3%淀粉溶液2mL,用0.1000mol•L-1Na2S2O3溶液滴定(发生:I2+2S2O32-═2I-+S4O62-)到终点时消耗12.00mL,试计算产品中Ca(IO3)2的质量分数(给出计算过程).

(1)若称取的I2质量为3.810g,为使I2充分氧化,则投料时KClO3的质量至少为3.675;同时生成的氯气体积为336mL(标准状况).
(2)用KOH溶液调节pH的目的是将KIO3•HIO3转变为KIO3.
(3)已知几种盐的溶解度(g/100g水)如下:
| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
| KCl | 28.1 | 31.2 | 34.2 | 40.1 | 45.8 | 51.3 |
| Ca(IO3)2 | 0.119 | 0.195 | 0.3071 | 0.520 | 0.621 | 0.669 |
| 碘酸钙存在形态 | 无水盐 | 一水合物 | 六水合物 |
| 稳定时的温度区域 | >57.5℃ | 32-57.5℃ | <32℃ |
(4)准确称取产品0.6000g于烧标中,加1:1高氯酸20mL,微热溶解后,冷却,配成250.00mL溶液.移取上述溶液50.00mL置于250mL碘量瓶中,加入1:1高氯酸2mL、3gKI(足量)(发生:IO3-+5I-+6H+═3I2+3H2O),盖上瓶盖,暗处放置3min,加50mL水,加入0.3%淀粉溶液2mL,用0.1000mol•L-1Na2S2O3溶液滴定(发生:I2+2S2O32-═2I-+S4O62-)到终点时消耗12.00mL,试计算产品中Ca(IO3)2的质量分数(给出计算过程).
