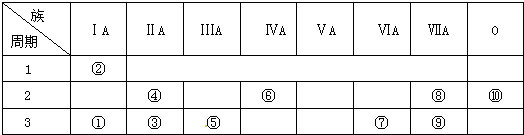
题目内容
下列各组物质相互混合反应,既有气体生成最终又有沉淀生成的是( )
①金属钠投入FeCl3溶液中 ②过量的NaOH溶液和明矾溶液③Na2S2O3溶液与稀硫酸 ④Na2O2投入FeCl2溶液中⑤浓硫酸铵溶液加入到浓氢氧化钠中 ⑥Al2(SO4)3与Na2SiO3溶液.
①金属钠投入FeCl3溶液中 ②过量的NaOH溶液和明矾溶液③Na2S2O3溶液与稀硫酸 ④Na2O2投入FeCl2溶液中⑤浓硫酸铵溶液加入到浓氢氧化钠中 ⑥Al2(SO4)3与Na2SiO3溶液.
| A、①②④ | B、③④⑤ |
| C、①③④⑥ | D、①③④ |
考点:钠的化学性质,含硫物质的性质及综合应用,钠的重要化合物,镁、铝的重要化合物,铁的氧化物和氢氧化物
专题:元素及其化合物
分析:①Na先和水反应,然后NaOH再和氯化铁发生复分解反应;②过量的NaOH溶液和明矾溶液生成偏铝酸钠;③Na2S2O3溶液与稀硫酸反应生成二氧化硫和S;④Na2O2投入FeCl2溶液中反应生成氢氧化铁沉淀和氧气;⑤浓硫酸铵溶液加入到浓氢氧化钠中生成氨气;⑥Al2(SO4)3与Na2SiO3溶液生成氢氧化铝和硅酸.
解答:
解:①Na先和水反应生成氢氧化钠和氢气,然后NaOH再和氯化铁发生复分解反应生成氢氧化铁沉淀,所以有气体和沉淀生成,故正确;
②过量的NaOH溶液和明矾溶液生成偏铝酸钠,溶液中最终没有沉淀生成,也没有气体,故错误;
③Na2S2O3溶液与稀硫酸反应生成二氧化硫气体和硫沉淀,所以有气体和沉淀生成,故正确;
④Na2O2投入FeCl2溶液中,过氧化钠把亚铁离子氧化为铁离子,过氧化钠与水反应生成氢氧化钠和氧气,氢氧化钠与铁离子反应生成氢氧化铁沉淀,所以有气体和沉淀生成,故正确;
⑤浓硫酸铵溶液加入到浓氢氧化钠中生成氨气,反应中只有气体生成,无沉淀,故错误;
⑥Al2(SO4)3与Na2SiO3溶液生成氢氧化铝和硅酸,反应中只有沉淀,没有气体生成,故错误;
所以正确的有①③④;
故选D.
②过量的NaOH溶液和明矾溶液生成偏铝酸钠,溶液中最终没有沉淀生成,也没有气体,故错误;
③Na2S2O3溶液与稀硫酸反应生成二氧化硫气体和硫沉淀,所以有气体和沉淀生成,故正确;
④Na2O2投入FeCl2溶液中,过氧化钠把亚铁离子氧化为铁离子,过氧化钠与水反应生成氢氧化钠和氧气,氢氧化钠与铁离子反应生成氢氧化铁沉淀,所以有气体和沉淀生成,故正确;
⑤浓硫酸铵溶液加入到浓氢氧化钠中生成氨气,反应中只有气体生成,无沉淀,故错误;
⑥Al2(SO4)3与Na2SiO3溶液生成氢氧化铝和硅酸,反应中只有沉淀,没有气体生成,故错误;
所以正确的有①③④;
故选D.
点评:本题考查了物质间的反应,明确物质的性质是解本题关键,根据物质的性质来分析解答,熟练掌握元素化合物之间的反应,题目难度不大.

练习册系列答案
相关题目
电解一定量的硫酸铜溶液的实验装置如图①,电解的实验数据如图②,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).则下列说法正确的是( )
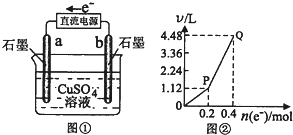

| A、开始时b电极有红色物质析出,而后有气泡产生 |
| B、a电极上的电子经溶液流向b极再流入直流电源 |
| C、曲线P~Q段表示产生H2和O2的体积比为1:2 |
| D、从开始到Q点收集到的混合气体中有0.1mol氧气 |
下列说法中正确的是( )
| A、凡能发生银镜反应的有机物一定是醛 |
| B、酸和醇发生的反应一定是酯化反应 |
| C、乙醇易溶于水是因为分子间形成了一种叫氢键的化学键 |
| D、在酯化反应中,羧酸脱去羧基中的羟基,醇脱去羟基中的氢而生成水和酯 |
有如下几种物质,①蔗糖②麦芽糖③甲酸甲酯④淀粉,水解前后都能发生银镜反应的( )
| A、①②③ | B、①③ |
| C、②③ | D、①②③④ |
下列各组分子中,都属于含极性键的非极性分子的是( )
| A、CO2 H2S |
| B、C60 C2H4 |
| C、C2H4 CH4 |
| D、NH3 HCl |