题目内容
既能与稀硫酸反应,又能与NaOH溶液反应的是( )
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3.
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3.
| A、①②③ | B、②③ |
| C、②④ | D、①②③④ |
考点:镁、铝的重要化合物
专题:几种重要的金属及其化合物
分析:根据物质的性质进行解答,既能与酸又能与碱反应的物质有:铝、两性氧化物、两性氢氧化物、弱酸酸式盐、弱酸的铵盐、氨基酸等.
解答:
解:①Al与硫酸生成硫酸铝、氢气和水、Al与氢氧化钠溶液生成偏铝酸钠、氢气和水,故①符合;
②氧化铝属于两性氧化物,与硫酸反应生成硫酸铝和水,氧化铝与氢氧化钠溶液生成偏铝酸钠和水,故②符合;
③氢氧化铝属于两性氧化物,与硫酸反应生成硫酸铝和水,氢氧化铝与氢氧化钠溶液生成偏铝酸钠和水,故③符合;
④碳酸氢钠属于弱酸的酸式盐,与硫酸反应生成硫酸钠与二氧化碳,与氢氧化钠反应生成碳酸钠,故④符合;
故选D.
②氧化铝属于两性氧化物,与硫酸反应生成硫酸铝和水,氧化铝与氢氧化钠溶液生成偏铝酸钠和水,故②符合;
③氢氧化铝属于两性氧化物,与硫酸反应生成硫酸铝和水,氢氧化铝与氢氧化钠溶液生成偏铝酸钠和水,故③符合;
④碳酸氢钠属于弱酸的酸式盐,与硫酸反应生成硫酸钠与二氧化碳,与氢氧化钠反应生成碳酸钠,故④符合;
故选D.
点评:本题考查元素化合物的性质,题目难度不大,旨在考查学生对知识的理解识记与知识归纳,注意归纳总结既能与酸又能与碱反应的物质.

练习册系列答案
相关题目
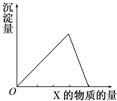 把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )
把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )| A、X为CO2,Y为Ca(OH)2 |
| B、X为NH3?H2O,Y为AlCl3 |
| C、X为NaOH,Y为AlCl3 |
| D、X为HCl,Y为Na[Al(OH)4] |
现有100mL只含MgCl2和AlCl3两种溶质的混合溶液,其中c(Cl-)=1.0mol?L-1,c(Mg2+)=0.35mol?L-1要使其中的Mg2+全部转化为Mg(OH)2沉淀而分离出来,至少需要2mol?L-1的NaOH溶液的体积是( )
| A、25mL | B、35mL |
| C、45mL | D、55mL |
检验未知溶液中是否含有硫酸根离子,合理的方法是( )
| A、只加入硝酸钡溶液 |
| B、加入氯化钡和氯化氢的混合溶液 |
| C、先加入氛化钡解液.再加入稀硝酸 |
| D、先加入稀盐酸,再加入氯化钡溶液 |
已知25℃时,KHF=7.2×10-4 KHCN=4.9×10-10 KHNO2=4.6×10-4 KCH3COOH=1.8×10-5则相同浓度的上述溶液中溶质分子浓度最大的是( )
| A、HF |
| B、HCN |
| C、HNO2 |
| D、CH3COOH |
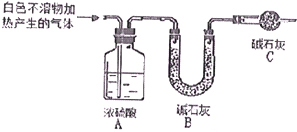 某研究性学习小组做实验做实验时偶然发现,表面擦去氧化膜的镁片可与NaHCO3溶液反应产生大量气体大量气体和白色不溶物,该小组同学通过如下实验,验证产物并探究反应原理.
某研究性学习小组做实验做实验时偶然发现,表面擦去氧化膜的镁片可与NaHCO3溶液反应产生大量气体大量气体和白色不溶物,该小组同学通过如下实验,验证产物并探究反应原理.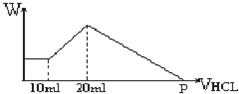 把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中后有0.58克白色沉淀,在所得浊液中,逐滴加入0.5mol/L的盐酸,加入盐酸的体积与生成沉淀的质量关系如图所示:
把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中后有0.58克白色沉淀,在所得浊液中,逐滴加入0.5mol/L的盐酸,加入盐酸的体积与生成沉淀的质量关系如图所示: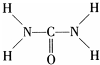 尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.
尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.