题目内容
2.下列各组物质熔化或升华时,所克服的粒子间作用属于同种类型的是( )| A. | MgO和SiC | B. | Fe和S | C. | CO2 和SiO2 | D. | 碘和干冰升华 |
分析 离子晶体熔化克服离子键,原子晶体熔化克服共价键,金属晶体熔化克服金属键,分子晶体熔化或升华克服分子间作用力,以此来解答.
解答 解:A.MgO熔化克服离子键、SiC熔化克服共价键,类型不同,故A不选;
B.S熔化克服分子间作用力,Fe熔化克服金属键,类型不同,故B不选;
C.CO2 熔化或升华克服分子间作用力,SiO2熔化克服共价键,类型不同,故C不选;
D.碘和干冰升华均克服分子间作用力,类型相同,故D选;
故选D.
点评 本题考查晶体类型及化学键,明确不同类型的晶体在熔化时克服不同的作用力是解答本题的关键,题目难度不大,注意把握晶体类型.

练习册系列答案
相关题目
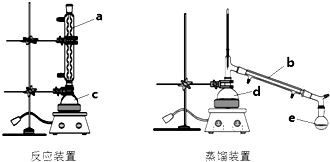
10.某化学兴趣小组利用如图装置进行乙酸乙酯合成和分离的实验探究,请回答以下问题
(1)写出合成乙酸乙酯的化学方程式CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.
(2)仪器b的名称冷凝管,图中起冷凝回流作用的是a(填a、b、c、d、e).
(3)为了提高乙酸乙酯的产率可采取的措施将CH3COOCH2CH3及时蒸馏分离;反应温度不宜过高,减少CH3COOHCH3CH2OH的挥发;反应物控制无水条件,浓硫酸的吸水作用有利于平衡向正反应方向移动,提高产率
(4)经过0.5h加热反应后,将反应装置c中粗产品转移至d中进行蒸馏
根据上表分析,蒸馏后得到的乙酸乙酯中,最有可能含有CH3CH2OH杂质.

(1)写出合成乙酸乙酯的化学方程式CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.(2)仪器b的名称冷凝管,图中起冷凝回流作用的是a(填a、b、c、d、e).
(3)为了提高乙酸乙酯的产率可采取的措施将CH3COOCH2CH3及时蒸馏分离;反应温度不宜过高,减少CH3COOHCH3CH2OH的挥发;反应物控制无水条件,浓硫酸的吸水作用有利于平衡向正反应方向移动,提高产率
(4)经过0.5h加热反应后,将反应装置c中粗产品转移至d中进行蒸馏
| 物质 | 98.3%浓硫酸 | 乙酸乙酯 | 乙酸 | 乙醇 | 乙醚 | 水 |
| 沸点 | 338℃, | 77.1℃ | 118℃ | 78.5℃ | 34.6℃ | 100℃ |
17.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理正确的是( )
| 50ml盐酸 | 50ml盐酸 | 50ml盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
| A. | 15.7g混合物能恰好与盐酸完全反应 | |
| B. | 根据表中数据不能计算出混合物中NaHCO3的质量分数 | |
| C. | 向50ml盐酸中加入混合物27.6g时,盐酸过量 | |
| D. | 盐酸的物质的量浓度为3.0mol/L |
14.在光照条件下,将CH4和Cl2按质量比16:71混合,充分反应后得到物质的量最多的产物是( )
| A. | CH3Cl | B. | CH2Cl2 | C. | CCl4 | D. | HCl |
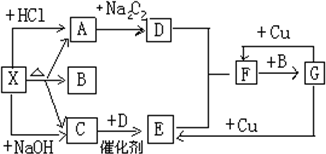 如图中的每一个方格表示有关的一种反应物或生成物,其中X为正盐,A能使澄清石灰水变浑浊的无色气体,C是能使湿润的红色的石蕊试纸变蓝的无色气体,
如图中的每一个方格表示有关的一种反应物或生成物,其中X为正盐,A能使澄清石灰水变浑浊的无色气体,C是能使湿润的红色的石蕊试纸变蓝的无色气体,