题目内容
9.在一真空固定体积的密闭容器中,充入10mol N2和30mol H2混合后发生反应:N2+3H2?2NH3.在一定温度下达到平衡,H2的转化率为80%.若在同一容器中充入NH3,欲使反应达到平衡时各成分的百分含量与上述平衡时相同,则起始时充入NH3的物质的量和达到平衡时NH3的转化率是( )| A. | 15mol 20% | B. | 20mol 20% | C. | 20mol 80% | D. | 40mol 80% |
分析 恒温恒容下,若开始只充入NH3,欲达到平衡时的各成份的百分含量与原平衡时相同,二者为等效平衡,由于反应前后气体的化学计量数之和不相等,故平衡时对应组分的物质的量相等,根据极限法计算氨气的物质的量,根据方程式计算原平衡时氨气的物质的量,进而计算开始只充入NH3时氨气的转化率.
解答 解:恒温恒容下,若开始只充入NH3,欲达到平衡时的各成份的百分含量与原平衡时相同,二者为等效平衡,由于反应前后气体的化学计量数之和不相等,故平衡时对应组分的物质的量相等,需要氨气的物质的量=10mol×2=20mol,原平衡中参加反应氢气为30mol×80%=24mol,由方程式可知平衡时氨气的物质的量=24mol×$\frac{2}{3}$=16mol,故若开始只充入NH3,氨气的转化率=$\frac{20mol-16mol}{20mol}$×100%=20%,
故选B.
点评 本题考查化学平衡计算、等效平衡,理解等效平衡规律是解题关键,注意不同方向建立等效平衡,转化率之和为1,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.二甲醚(CH3OCH3)是一种应用前景广阔的清洁燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
回答下列问题:
(1)该工艺的总反应为3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H,该反应△H=-263 kJ•mol-1,化学平衡常数K=K12•K2•K3(用含K1、K2、K3的代数式表示);
(2)下列措施中,能提高CH3OCH3产率的有AD;
A.分离出二甲醚 B.升高温度
C.改用高效催化剂 D.增大压强
(3)工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生.该工艺中反应③的发生提高了CH3OCH3的产率,原因是反应③消耗了反应②中的产物H2O,使反应②的化学平衡向正反应方向移动,从而提高CH3OCH3的产率;
(4)以n(H2)/n(CO)=2 通入1L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示.下列说法正确的是CD;
A.该反应的△H>0
B.若在p2和316℃时反应达到平衡,则CO的转化率小于50%
C.若在p3和316℃时反应达到平衡,H2的转化率等于50%
D.若在p3和316℃时,起始时n(H2)/n(CO)=3,则达平衡时CO的转化率大于50%
(5)某温度下,将8.0mol H2和4.0mol CO充入容积为2L的密闭容器中,发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g),反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数K=2.25.
| 编号 | 热化学方程式 | 化学平衡常数 |
| ① | CO(g)+2H2(g)?CH3OH(g)△H1=-99kJ•mol-1 | K1 |
| ② | 2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24kJ•mol-1 | K2 |
| ③ | CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41kJ•mol-1 | K3 |
(1)该工艺的总反应为3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H,该反应△H=-263 kJ•mol-1,化学平衡常数K=K12•K2•K3(用含K1、K2、K3的代数式表示);
(2)下列措施中,能提高CH3OCH3产率的有AD;
A.分离出二甲醚 B.升高温度
C.改用高效催化剂 D.增大压强
(3)工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生.该工艺中反应③的发生提高了CH3OCH3的产率,原因是反应③消耗了反应②中的产物H2O,使反应②的化学平衡向正反应方向移动,从而提高CH3OCH3的产率;
(4)以n(H2)/n(CO)=2 通入1L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示.下列说法正确的是CD;
A.该反应的△H>0
B.若在p2和316℃时反应达到平衡,则CO的转化率小于50%
C.若在p3和316℃时反应达到平衡,H2的转化率等于50%
D.若在p3和316℃时,起始时n(H2)/n(CO)=3,则达平衡时CO的转化率大于50%

(5)某温度下,将8.0mol H2和4.0mol CO充入容积为2L的密闭容器中,发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g),反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数K=2.25.
20.一定量的Fe与过量的稀硫酸反应制取氢气,一定温度下为加快反应速率而又不影响氢气的量,可向其中加入( )
| A. | KCl晶体 | B. | Zn粉 | C. | SO3固体 | D. | CuSO4晶体 |
4. 一种碳纳米管能够吸附氢气,用这种材料制备的二次电池原理如图所示,该电池的电解质为6mol•L - 1KOH溶液,下列说法中正确的是( )
一种碳纳米管能够吸附氢气,用这种材料制备的二次电池原理如图所示,该电池的电解质为6mol•L - 1KOH溶液,下列说法中正确的是( )
 一种碳纳米管能够吸附氢气,用这种材料制备的二次电池原理如图所示,该电池的电解质为6mol•L - 1KOH溶液,下列说法中正确的是( )
一种碳纳米管能够吸附氢气,用这种材料制备的二次电池原理如图所示,该电池的电解质为6mol•L - 1KOH溶液,下列说法中正确的是( )| A. | 放电时K +移向负极 | |
| B. | 放电时电池负极的电极反应为H 2-2e -═2H + | |
| C. | 放电时电池正极的电极反应为NiO(OH)+H 2O+e -═Ni(OH) 2+OH - | |
| D. | 该电池充电时将碳电极与电源的正极相连,发生氧化反应 |
1.对下列溶液的说法正确的是( )
| A. | pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 | |
| B. | 浓度均为0.1 mol/L的四种溶液中由水电离出的H+浓度由大到小的顺序是:氯化铵、醋酸、硫酸、氢氧化钠 | |
| C. | 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12.某溶液中含有Cl-和CrO42-,浓度均为0.010mol•L-1,向该溶液中逐滴加入0.010 mol•L-1的AgNO3溶液时,CrO42-先沉淀 | |
| D. | 25℃时,取0.2mol•L-1 HClO溶液与0.2mol•L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则c(Na+)-c(ClO-)=9.9×10-7mol•L-1 |
18.下列装置或操作能达到实验目的是( )
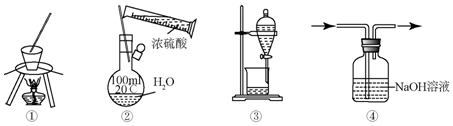

| A. | ①用于实验室从食盐水中提取氯化钠 | |
| B. | ②配制一定物质的量浓度的硫酸溶液 | |
| C. | ③用于苯萃取碘水中的碘后放出碘的苯溶液 | |
| D. | ④用于除去CO中混有的CO2 |