题目内容
9.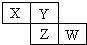 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的L层电子是K层电子数的3倍,下列说法不正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的L层电子是K层电子数的3倍,下列说法不正确的是( )| A. | Y的气态氢化物比X的稳定 | |
| B. | W的最高价氧化物对应水化物的酸性比Z的强 | |
| C. | Y的非金属性比Z的强 | |
| D. | X与Y形成的化合物都易溶于水 |
分析 X、Y、Z均为短周期元素,Y原子的L层电子是K层电子数的3倍,则Y的第一层电子数为2,最外层电子数为6,所以Y应为O,结合位置可知,Z为S,X为N,W为Cl,并利用元元素周期律来解答.
解答 解:X、Y、Z均为短周期元素,Y原子的L层电子是K层电子数的3倍,则Y的第一层电子数为2,最外层电子数为6,所以Y应为O,结合位置可知,Z为S,X为N,W为Cl.
A.同周期元素从左到右元素的非金属性逐渐增大,Y的气态氢化物的稳定性比X的强,故A正确;
B.同周期元素从左到右元素的非金属性逐渐增大,则非金属性Cl>S,所以最高价氧化物对应水化物的酸性W比Z强,故B正确;
C.同主族从上到下非金属性逐渐减弱,则非金属性O>S,故C正确;
D.X与Y形成的化合物可以是一氧化氮,一氧化氮不溶于水,故D错误;
故选D.
点评 本题考查位置、结构、性质的应用,Y为解答本题的突破口,元素的推断及熟悉元素同期律是解答本题的关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.下列说法中正确的是( )
| A. | SO2、CO2、SiO2中的S、C、Si均为sp3杂化 | |
| B. | SO32-、CO32-、SiO32-均为平面三角形 | |
| C. | H3O+、NH4+、[Cu(NH3)4]2+均含有配位键 | |
| D. | 石墨、新型高分子导电材料聚乙炔、金属晶体均含有金属键 |
20.反应2SO2(g)+O2(g)═2SO3(g)经一段时间后,SO3的浓度增加了0.4mol•L-1,在这段时间内用O2表示的反应速率为0.04mol•L-1•s-1,则这段时间为C( )
| A. | 0.1s | B. | 2.5s | C. | 5s | D. | 10s |
17.下列气体中,无色而有刺激性气味的是( )
| A. | N2 | B. | NO | C. | SO2 | D. | NO2 |
4.下列有关物质与其用途不相对应的是( )
| A. | 氮化硅陶瓷--导热剂 | B. | Si和Ge--半导体材料 | ||
| C. | 钢化玻璃--汽车窗玻璃 | D. | SiO2--制光纤 |
14.根据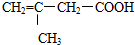 的结构,它不可能发生的反应是( )
的结构,它不可能发生的反应是( )
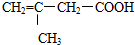 的结构,它不可能发生的反应是( )
的结构,它不可能发生的反应是( )| A. | 与银氨溶液反应析出银 | |
| B. | 使溴的四氯化碳溶液褪色 | |
| C. | 与乙醇在浓硫酸催化下发生酯化反应 | |
| D. | 与新制氢氧化铜反应 |
10.下列离子方程式书写正确的是( )
| A. | 氯气溶于水:H2O+Cl2═2H++ClOˉ+Clˉ | |
| B. | 锌片插入稀H2SO4溶液中:Zn+2H+═Zn2++H2↑ | |
| C. | 氢氧化钡溶液与稀硫酸反应:H++SO42-+OH-+Ba2+═H2O+BaSO4↓ | |
| D. | 碳酸钙溶于稀盐酸:CO32-+2H+═H2O+CO2↑ |

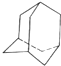 油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:
油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示: