题目内容
高锰酸钾是锰的重要化合物,也是中学化学实验中常用的试剂.以下是实验室中模拟工业上用软锰矿制备高锰酸钾的部分流程图.
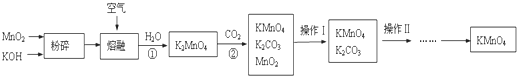
(1)操作Ⅰ的名称为 .反应②的化学方程式为 .
(2)制备KMnO4也可以用电解法.用Pt作阳极,Fe作阴极,K2MnO4为电解液,阳极的电极反应式为 .
(3)KMnO4在酸性介质中的强氧化性广泛应用于化学实验中.
例如:2KMnO4+3H2SO4+5Na2SO3=5Na2SO4+K2SO4+2MnSO4+3H2O.某同学用KMnO4测定实验室长期存放的Na2SO3固体的纯度.现准确称取6.3g Na2SO3固体样品,配成500mL溶液.取25.00mL上述溶液放入锥形瓶中,用0.01000mol/L 的酸性KMnO4溶液进行滴定.滴定结果如下表所示:
①配制500mLNa2SO3溶液时,必须用到的实验仪器有:烧杯、玻璃棒、托盘天平、药匙和 、 .
②判断滴定终点的依据是 .
③用上述实验数据,计算Na2SO3的纯度为 .
(4)25℃时,已知Ksp[Mn(OH)2]=2.06×10-13,则室温时,0.01mol/L氢氧化钠溶液中,锰离子的浓度最大可达到 mol/L.

(1)操作Ⅰ的名称为
(2)制备KMnO4也可以用电解法.用Pt作阳极,Fe作阴极,K2MnO4为电解液,阳极的电极反应式为
(3)KMnO4在酸性介质中的强氧化性广泛应用于化学实验中.
例如:2KMnO4+3H2SO4+5Na2SO3=5Na2SO4+K2SO4+2MnSO4+3H2O.某同学用KMnO4测定实验室长期存放的Na2SO3固体的纯度.现准确称取6.3g Na2SO3固体样品,配成500mL溶液.取25.00mL上述溶液放入锥形瓶中,用0.01000mol/L 的酸性KMnO4溶液进行滴定.滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00mL | 0.02 | 24.01 |
| 2 | 25.00mL | 0.70 | 24.71 |
| 3 | 25.00mL | 0.20 | 24.20 |
②判断滴定终点的依据是
③用上述实验数据,计算Na2SO3的纯度为
(4)25℃时,已知Ksp[Mn(OH)2]=2.06×10-13,则室温时,0.01mol/L氢氧化钠溶液中,锰离子的浓度最大可达到
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验评价题
分析:二氧化锰与氢氧化钾粉碎在空气中熔融,加水溶解得到K2MnO4溶液,通入二氧化碳得到KMnO4、MnO2、K2CO3,过滤除去滤渣(MnO2),滤液为KMnO4、K2CO3溶液,浓缩结晶,趁热过滤得到KMnO4晶体,滤液中含有K2CO3,在滤液中加氢氧化钙得到碳酸钙沉淀和KOH;
(1)操作Ⅰ是分离溶液和难溶物的实验操作为过滤;,反应②通入二氧化碳得到KMnO4、MnO2、K2CO3的反应,依据原子守恒配平书写化学方程式;
(2)在电解槽中用铂板作用阳极,铁作阴极电解K2MnO4溶液得到KMnO4,阴极上水得电子发生还原反应生成氢气和氢氧根离子,阳极上锰酸根离子失电子反应氧化反应生成高锰酸根离子;
(3)①配制溶液的实验步骤和注意问题分析选择需要的仪器;
②酸性KMnO4溶液进行滴定亚硫酸钠溶液,滴入最后一滴,溶液呈紫红色且半分钟不变化,证明反应达到终点;
③计算25ml溶液消耗高锰酸钾溶液平均体积,结合化学方程式定量关系计算得到250ml溶液中亚硫酸钠物质的量,得到质量分数;
(4)依据溶度积常数计算分析.
(1)操作Ⅰ是分离溶液和难溶物的实验操作为过滤;,反应②通入二氧化碳得到KMnO4、MnO2、K2CO3的反应,依据原子守恒配平书写化学方程式;
(2)在电解槽中用铂板作用阳极,铁作阴极电解K2MnO4溶液得到KMnO4,阴极上水得电子发生还原反应生成氢气和氢氧根离子,阳极上锰酸根离子失电子反应氧化反应生成高锰酸根离子;
(3)①配制溶液的实验步骤和注意问题分析选择需要的仪器;
②酸性KMnO4溶液进行滴定亚硫酸钠溶液,滴入最后一滴,溶液呈紫红色且半分钟不变化,证明反应达到终点;
③计算25ml溶液消耗高锰酸钾溶液平均体积,结合化学方程式定量关系计算得到250ml溶液中亚硫酸钠物质的量,得到质量分数;
(4)依据溶度积常数计算分析.
解答:
解:二氧化锰与氢氧化钾粉碎在空气中熔融,加水溶解得到K2MnO4溶液,通入二氧化碳得到KMnO4、MnO2、K2CO3,过滤除去滤渣(MnO2),滤液为KMnO4、K2CO3溶液,浓缩结晶,趁热过滤得到KMnO4晶体,滤液中含有K2CO3,在滤液中加氢氧化钙得到碳酸钙沉淀和KOH;
(1)操作Ⅰ是分离溶液和难溶物的实验操作为过滤;反应②通入二氧化碳得到KMnO4、MnO2、K2CO3的反应,依据原子守恒配平书写化学方程式3K2MnO4+2 CO2=2 KMnO4+2K2CO3+MnO2↓;
故答案为:过滤;3K2MnO4+2 CO2=2 KMnO4+2K2CO3+MnO2↓;
(2)电解锰酸钾溶液时,阴极上水得电子生成氢气和氢氧根离子,电极反应为2H2O+2e-═H2↑+2OH-,阳极上锰酸根离子失电子生成高锰酸根离子,电极反应式为2MnO42--2e-═2MnO4-,
故答案为:2MnO42--2e-═2MnO4-;
(3)①依据配制500mLNa2SO3溶液的操作步骤分析,必须用到的实验仪器有:烧杯、玻璃棒、托盘天平、药匙、500 mL容量瓶 胶头滴管;
故答案为:500 mL容量瓶;胶头滴管;
②酸性KMnO4溶液进行滴定亚硫酸钠溶液,滴入最后一滴,溶液呈紫红色且半分钟不变化,证明反应达到终点;
故答案为:锥形瓶溶液从无色变为浅红色,且半分钟内不褪去;
③标准溶液体积平均为=
=24ml,依据化学方程式定量关系计算
2KMnO4+3H2SO4+5Na2SO3=5Na2SO4+K2SO4+2MnSO4+3H2O.
2 5
0.024L×0.01000mol/L n
n=0.0006mol
250ml溶液中含有Na2SO3物质的量=0.0006mol×
=0.012mol
6.3g Na2SO3固体样品中亚硫酸钠质量分数=
×100%=24%;
故答案为:24%;
(4)25℃时,已知Ksp[Mn(OH)2]=2.06×10-13,则室温时,0.01mol/L氢氧化钠溶液中,Ksp[Mn(OH)2]=c(Mn2+)c2(OH-)=2.06×10-13,锰离子的浓度最大可达到c(Mn2+)=
=2.06×10-9mol/L,
故答案为:2.06×10-9.
(1)操作Ⅰ是分离溶液和难溶物的实验操作为过滤;反应②通入二氧化碳得到KMnO4、MnO2、K2CO3的反应,依据原子守恒配平书写化学方程式3K2MnO4+2 CO2=2 KMnO4+2K2CO3+MnO2↓;
故答案为:过滤;3K2MnO4+2 CO2=2 KMnO4+2K2CO3+MnO2↓;
(2)电解锰酸钾溶液时,阴极上水得电子生成氢气和氢氧根离子,电极反应为2H2O+2e-═H2↑+2OH-,阳极上锰酸根离子失电子生成高锰酸根离子,电极反应式为2MnO42--2e-═2MnO4-,
故答案为:2MnO42--2e-═2MnO4-;
(3)①依据配制500mLNa2SO3溶液的操作步骤分析,必须用到的实验仪器有:烧杯、玻璃棒、托盘天平、药匙、500 mL容量瓶 胶头滴管;
故答案为:500 mL容量瓶;胶头滴管;
②酸性KMnO4溶液进行滴定亚硫酸钠溶液,滴入最后一滴,溶液呈紫红色且半分钟不变化,证明反应达到终点;
故答案为:锥形瓶溶液从无色变为浅红色,且半分钟内不褪去;
③标准溶液体积平均为=
| 24.01-0.02+24.71-0.7+24.2-0.2 |
| 3 |
2KMnO4+3H2SO4+5Na2SO3=5Na2SO4+K2SO4+2MnSO4+3H2O.
2 5
0.024L×0.01000mol/L n
n=0.0006mol
250ml溶液中含有Na2SO3物质的量=0.0006mol×
| 500 |
| 25 |
6.3g Na2SO3固体样品中亚硫酸钠质量分数=
| 0.012mol×126g/mol |
| 6.3g |
故答案为:24%;
(4)25℃时,已知Ksp[Mn(OH)2]=2.06×10-13,则室温时,0.01mol/L氢氧化钠溶液中,Ksp[Mn(OH)2]=c(Mn2+)c2(OH-)=2.06×10-13,锰离子的浓度最大可达到c(Mn2+)=
| 2.06×10-13 |
| 0.012 |
故答案为:2.06×10-9.
点评:本题考查了物质提纯方法,溶液配制电解原理的分析应用,氧化还原反应滴定实验过程分析和计算方法的分析,掌握基础是关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某物质可能有甲酸、乙酸、甲醇和甲酸乙酯四种物质中的一种或几种,在鉴定时有下列现象:下列叙述正确的是( )
①有银镜反应,
②加入新制Cu(OH)2悬浊液沉淀不溶解,
③与含酚酞的NaOH溶液共热,发现溶液中红色逐渐褪去以至无色.
①有银镜反应,
②加入新制Cu(OH)2悬浊液沉淀不溶解,
③与含酚酞的NaOH溶液共热,发现溶液中红色逐渐褪去以至无色.
| A、几种物质都有 |
| B、有甲酸乙酯和甲酸 |
| C、有甲酸乙酯和甲醇 |
| D、有甲酸乙酯,可能有甲醇 |
某学生将一氯丙烷和NaOH溶液共热煮沸几分钟后,冷却,滴入AgNO3溶液,结果未见到白色沉淀生成,其主要原因是( )
| A、加热时间太短 |
| B、不应冷却后再滴入AgNO3溶液 |
| C、加AgNO3溶液后未加稀HNO3 |
| D、加AgNO3溶液前未用稀HNO3 |
下列实验或操作能达到目的是( )
| A、用饱和Na2CO3溶液鉴别乙醇、乙酸和乙酸乙酯 |
| B、除去苯中少量苯酚,向混合物种加入适量的溴水后过滤 |
| C、用乙醇萃取溴水中的溴,分液时有机层从分液漏斗上口倒出 |
| D、直接向溴乙烷水解后的溶液中加入AgNO3溶液以检验溴离子 |
既能跟盐酸反应,又能跟氢氧化钠溶液反应的氧化物是( )
| A、NaHCO3 |
| B、Al(OH)3 |
| C、NaAlO2 |
| D、Al2O3 |