题目内容
13.下列实验方案中,能达到实验目的是( )| 选项 | 实验目的 | 实验方案 |
| A | 配制100mL1.0mol/LCuSO4溶液 | 将25g CuSO4•5H2O溶于100mL蒸馏水中 |
| B | 除去CuO中混有的Al2O3 | 加入过量NaOH溶液后,过滤、洗涤、干燥 |
| C | 证明氧化性:H2O2>Fe3+ | 强硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 |
| D | 证明非金属性:Cl>C | 向NaHCO3溶液中加入过量盐酸振荡、静置、观察 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溶于100mL蒸馏水,为溶剂的体积;
B.氧化铝与NaOH反应,而CuO不能;
C.酸性条件下硝酸根离子可氧化亚铁离子;
D.NaHCO3溶液中加入过量盐酸,可知酸性盐酸大于碳酸,但盐酸为无氧酸.
解答 解:A.溶于100mL蒸馏水,为溶剂的体积,配制1mol/L溶液100mL时,溶液体积为100mL,故A错误;
B.氧化铝与NaOH反应,而CuO不能,则反应后过滤可除杂,故B正确;
C.酸性条件下硝酸根离子可氧化亚铁离子,不能确定过氧化氢与亚铁离子反应,故C错误;
D.NaHCO3溶液中加入过量盐酸,可知酸性盐酸大于碳酸,但盐酸为无氧酸,则不能比较Cl、C的非金属性,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握溶液的配制、混合物分离提纯、氧化性及非金属性比较、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
6.下列实验的操作、现象和解释或结论都正确的是( )
| 操作 | 现象 | 解释或结论 | |
| A | 将饱和Na2SO4溶液加入到饱和石灰水 | 有白色沉淀 | 有Na2SO4晶体析出 |
| B | 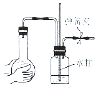 | 试剂瓶中有一段稳定水柱 | 装置气密性良好 |
| C | 将Al2(SO4)3溶液蒸干 | 有白色固体生成 | A13+水解生成Al(OH)3 |
| D |  | 锥形瓶溶液产生淡黄色沉淀 | 苯与溴发生取代反应 |
| A. | A | B. | B | C. | C | D. | D |
7.分子式为C6H12O2且能与小苏打溶液反应放出气体的有机物共有几种(不考虑立体异构)( )
| A. | 4 | B. | 6 | C. | 8 | D. | 10 |
2.扁桃酸衍生物是重要的医药中间体,在合成该有机物的过程中涉及如图转化:
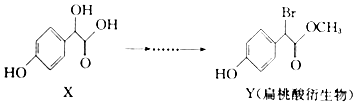
下列说法正确的是( )

下列说法正确的是( )
| A. | 化合物X的分子式为C8H8O4 | |
| B. | 化合物X、Y均可与NaHCO3溶液反应生成CO2 | |
| C. | 化合物X、Y分子中均含有1个手性碳原子 | |
| D. | 在一定条件下,化合物Y可发生加成反应和消去反应 |
8.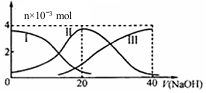 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )
 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )| A. | 当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(A2-)>c(H+)>c(HA-)>c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水的大 | |
| C. | 当V(NaOH)=30 mL时,溶液中存在以下关系:2c(H+)+3c(H2A)+c(HA-)=c(A2-)+2c(OH-) | |
| D. | 向NaHA溶液加入水的过程中,pH可能增大也可能减小 |
18.下列物质属于电解质的是( )
| A. | CO2 | B. | Ca(OH)2 | C. | 食盐水 | D. | 石墨 |
5.一定条件下,0.3molX(g)与Y(g)在容积固定的密闭容器中发生反应:X(g)+3Y(g)?2Z(g),△H=-aKJ/mol,下列说法正确的是( )
| A. | 反应一段时间后,X与Y的物质的量之比仍为1:1 | |
| B. | 达到平衡时,且反应放出0.1aKJ的热量 | |
| C. | 达到平衡后,若向平衡体系中充入稀有气体,Z的正反应速率将不发生变化 | |
| D. | X的体积分数保持不变,说明反应已达到平衡 |
2.设NA为阿伏伽德罗常数,下列说法正确的是( )
| A. | 1L1mol/L的盐酸溶液中,所含HCl分子数为NA | |
| B. | 常温常压下,71gCl2溶于水,转移的电子数目为0.1NA | |
| C. | 标准状况下,22.4LSO2和SO3的混合物,含硫原子的数目为NA | |
| D. | 0.5mol乙醇中含有的极性共价键数目为3.5NA |
4.然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的 ( )
| A. | NaOH | B. | NH3•H2O | C. | CuO | D. | Cu(OH)2 |