题目内容
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,2.24L甲醇中含有NA个碳原子 |
| B、在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4 NA |
| C、常温常压下,1mol C10H22分子中含有共价键的数目为31NA |
| D、用含有0.1molFeCl3的饱和溶液制得的氢氧化铁胶体中胶粒数等于0.1NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、标况下,甲醇为液态;
B、根据Na2O2与H2O的反应为歧化反应来分析;
C、根据烷烃中的碳原子之间是碳碳单键来分析;
D、一个氢氧化铁胶粒是多个氢氧化铁的聚集体.
B、根据Na2O2与H2O的反应为歧化反应来分析;
C、根据烷烃中的碳原子之间是碳碳单键来分析;
D、一个氢氧化铁胶粒是多个氢氧化铁的聚集体.
解答:
解:A、标况下,甲醇为液态,故A错误;
B、Na2O2与H2O的反应为歧化反应:2Na2O2+2H2O=4NaOH+O2↑,此反应转移2mol电子,生成1molO2,故当生成0.1 mol氧气时,转移电子的物质的量为0.2mol,数目为0.2NA,故B错误;
C、烷烃中的碳原子之间是碳碳单键,则1mol C10H22分子中含9mol碳碳单键,22mol碳氢键,故共价键的物质的量共为31mol,数目为31NA,故C正确;
D、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故0.1molFeCl3的饱和溶液制得的氢氧化铁胶体中胶粒数小于0.1NA,故D错误.
故选C.
B、Na2O2与H2O的反应为歧化反应:2Na2O2+2H2O=4NaOH+O2↑,此反应转移2mol电子,生成1molO2,故当生成0.1 mol氧气时,转移电子的物质的量为0.2mol,数目为0.2NA,故B错误;
C、烷烃中的碳原子之间是碳碳单键,则1mol C10H22分子中含9mol碳碳单键,22mol碳氢键,故共价键的物质的量共为31mol,数目为31NA,故C正确;
D、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故0.1molFeCl3的饱和溶液制得的氢氧化铁胶体中胶粒数小于0.1NA,故D错误.
故选C.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
相关题目
可逆反应mA(气)?nB(气)达到平衡时,下列叙述中正确的是( )
①V(正)=V(逆)≠0
②A的生成速成率等于A的分解速率
③A与B的物质的量不变
④A与B的生成速率之比为m:n.
①V(正)=V(逆)≠0
②A的生成速成率等于A的分解速率
③A与B的物质的量不变
④A与B的生成速率之比为m:n.
| A、① | B、①② | C、①③ | D、①②③④ |
两瓶体积相等的气体,一瓶是NO,另一瓶是N2和O2,同温同压时瓶内气体的关系一定正确的是( )
| A、所含原子数相等 |
| B、气体密度相等 |
| C、气体质量相等 |
| D、摩尔质量相等 |
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,2.24L水中所含的电子数为NA |
| B、常温常压下,16g O3所含的原子数为NA |
| C、0.1molNa2O2晶体中所含的离子数为0.4NA |
| D、1molFe在氧气中充分燃烧失去的电子数为3NA |
跟50mL 1mol/L HCl溶液中H+离子的物质的量浓度相同的溶液是( )
| A、50 mL 1 mol/L醋酸溶液 |
| B、100 mL 0.5 mol/L硫酸溶液 |
| C、100 mL 0.25 mol/L硫酸溶液 |
| D、200 mL 1 mol/L硝酸溶液 |
下列化学用语错误的是( )
A、氟离子的结构示意图: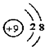 |
B、-CH3的电子式: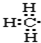 |
C、Na+的电子排布图: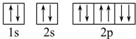 |
| D、Na的简化电子排布式:[Ne]3s1 |
不能说明醋酸是弱电解质的事实是( )
| A、醋酸溶液的导电性比盐酸弱 |
| B、向醋酸钠溶液中通入少量氯化氢,c(CH3COO-)减小 |
| C、0.1 mol/L的醋酸溶液的pH约为3 |
| D、pH=1的醋酸溶液用水稀释1000倍后,pH<4 |
下列说法不正确的是( )
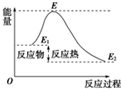

| A、反应物分子(或离子)间的每次碰撞是反应的先决条件 |
| B、反应物的分子的每次碰撞都能发生化学反应 |
| C、活化分子具有比普通分子更高的能量,催化剂能够减低活化能的数值 |
| D、活化能是活化分子的平均能量与所有分子平均能量之差,如图所示正反应的活化能为E-E1 |