题目内容
不能用有关胶体的观点解释的现象是( )
| A、在河流人海口处易形成三角洲 |
| B、在NaHCO3溶液中滴入CaCl2溶液,看不到沉淀 |
| C、少许FeCl3饱和溶液逐滴滴入沸水中,看不到红褐色沉淀 |
| D、同一支钢笔,同时使用不同牌号的墨水易发生堵塞 |
考点:分散系、胶体与溶液的概念及关系
专题:溶液和胶体专题
分析:胶体是分散质粒子介于1-100nm之间的分散系,不能够透过半透膜,胶体因为吸附带电离子形成带电的胶体微粒,胶体中加入可溶性电解质或者带相反电荷的胶体微粒会发生聚沉,据此解答.
解答:
解:A.江河中的泥沙属于胶体分散系,江河入海口三角洲的形成与胶体的聚沉性质有关,故A不选;
B.在NaHCO3溶液中滴入CaCl2溶液,看不到沉淀,是因为NaHCO3和CaCl2不符合复分解反应发生的条件,两者不反应,与胶体性质无关,故B选;
C.少许FeCl3饱和溶液逐滴滴入沸水中,会生成氢氧化铁胶体,故看不到沉淀,与胶体是介穏体系有关,故C不选;
D.不同牌号的墨水属于不同胶体,混合使用会发生聚沉,故D不选;
故选:B.
B.在NaHCO3溶液中滴入CaCl2溶液,看不到沉淀,是因为NaHCO3和CaCl2不符合复分解反应发生的条件,两者不反应,与胶体性质无关,故B选;
C.少许FeCl3饱和溶液逐滴滴入沸水中,会生成氢氧化铁胶体,故看不到沉淀,与胶体是介穏体系有关,故C不选;
D.不同牌号的墨水属于不同胶体,混合使用会发生聚沉,故D不选;
故选:B.
点评:本题考查了胶体的性质,题目难度不大,熟悉胶体的性质是解题关键,注意胶体聚沉发生的条件和应用.

练习册系列答案
相关题目
关于下列装置说法正确的是( )
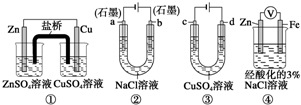

| A、装置②工作一段时间后,a极附近溶液的pH增大 |
| B、用装置③精炼铜时,c极为粗铜 |
| C、装置①中,盐桥中的K+移向ZnSO4溶液 |
| D、装置④中电子由Zn流向Fe,装置中有Fe2+生成 |
铝条与稀盐酸反应时,下列因素不会影响氢气产生速率的是( )
| A、盐酸的浓度 |
| B、铝条的表面积 |
| C、溶液的温度 |
| D、加少量Na2SO4 |
同温同压下,等质量的下列气体物质的量最大的是( )
| A、O2 |
| B、CH4 |
| C、CO2 |
| D、SO2 |
在一个容积固定的密闭容器中充入1molHI,建立如下平衡:H2(g)+I2(g)?2HI(g),测得HI的转化率为a%.其他条件不变,在上述平衡体系中再充入1molHI,待平衡建立时HI的转化率为b%,则a、b的关系为( )
| A、a>b | B、a<b |
| C、a=b | D、无法确定 |
下列离子方程式书写正确的是( )
| A、氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
| B、KAl(SO4)2中滴加Ba(OH)2使SO42-恰好完全沉淀2Al3++3 SO42-+3 Ba2++6 OH-=2Al(OH)3↓+3BaSO4↓ |
| C、将少量硝酸银溶液滴入氨水中:Ag++2NH3?H2O═[Ag(NH3)2]++2H2O |
| D、碳酸氢钠溶液中加入过量的石灰水:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
下列说法正确的是( )
| A、Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得 |
| B、金属与盐溶液反应都是置换反应 |
| C、液氨、液氯、液态氯化氢都是非电解质 |
| D、凡能电离出氢离子的化合物都是酸 |
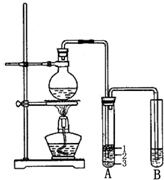 实验室制取少量溴乙烷的装置如图所示.
实验室制取少量溴乙烷的装置如图所示.