题目内容
|
(创新)2009年2月4日,抚顺百吨液化石油气发生泄漏,形成3万立方米白茫茫的毒雾气体,笼罩在6平方公里的土地上.你认为这白茫茫的气体是
| |
| [ ] | |
A. |
一种纯净物 |
B. |
全部由无机化合物组成的混合物 |
C. |
全部由有机化合物组成的混合物 |
D. |
由无机化合物和有机化合物组成的混合物 |
答案:D
解析:
解析:
|
由炼厂气所得的液化石油气的主要成分为丙烷、丙烯、丁烷、丁烯,同时含有少量的戊烷、戊烯和微量硫化物杂质.故此气体应该是无机化合物和有机化合物组成的混合物. |

练习册系列答案
相关题目

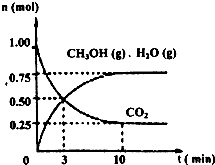 2009年12月7日一18日在丹麦首都哥本哈根召开的联合国气候会议,就未来应对气候变化的全球行动签署新的协议.而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.
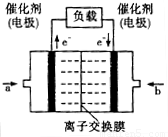
2009年12月7日一18日在丹麦首都哥本哈根召开的联合国气候会议,就未来应对气候变化的全球行动签署新的协议.而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.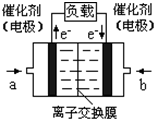 意图,则a处通入的是
意图,则a处通入的是
 (H2)=_______。
(H2)=_______。
 (H2)=_______。
(H2)=_______。 HCO3-+H+的电离平衡常数K=________。(已知:10-5.6=2.5×10-6)。
HCO3-+H+的电离平衡常数K=________。(已知:10-5.6=2.5×10-6)。