题目内容
11.草酸晶体的化学式可表示为H2C2O4•xH2O,为测定x值进行下列实验:(1)称取wg草酸晶体,配成100.00mL溶液.
(2)取25.00mL所配溶液置于锥形瓶中,加入适量稀硫酸后,用浓度为a mol/LKMnO4溶液滴定.KMnO4+H2C2O4+H2SO4→K2SO4+MnSO4+CO2↑+H2O(未配平)
回答下列问题:
①滴定时,KMnO4溶液应盛在酸式(填酸式或碱式)滴定管中;
②若滴定用的KMnO4溶液因放置而变质,浓度偏低,则根据实验求出的x值偏低(填偏高、偏低或无影响);
③滴定终点时,锥形瓶内溶液颜色变化是无色变成紫色,且半分钟不褪色;
④若滴定终点时,共用去KMnO4溶液V mL,求x的值为$\frac{59W}{9aV}-5$.
分析 ①高锰酸钾具有强氧化性,会腐蚀橡胶管,应装在酸式滴定管中;
②若KMnO4溶液变质,则消耗其体积偏大,所得x值偏小;
③滴定终点时溶液颜色无色变化为紫色且在30s内颜色不再恢复为原来颜色,证明反应达到终点;
④令草酸的浓度为cmol/L,根据反应方程式计算;
根据草酸的质量计算水的质量,结合关系式H2C2O4•xH2O~H2C2O4 ~xH2O计算x的值.
解答 解:①高锰酸钾具有强氧化性,会腐蚀橡胶管,应装在酸式滴定管中,故答案为:酸式滴定管;
②若KMnO4溶液变质,则消耗其体积偏大,所得x值偏小,故答案为:偏低;
③KMnO4溶液呈紫色,草酸反应完毕,当滴入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点;
故答案为:无色变成紫色,且半分钟不褪色;
④KMnO4 ~5H2C2O4
2mol 5mol
aV×10-3mol 0.025L×cmol/L
解得:c=0.1aVmol•L-1
H2C2O4•xH2O~H2C2O4 ~xH2O
1mol 18xg
0.1aV×0.1 W-0.1aV×0.1×90
解得x=$\frac{59W}{9aV}-5$,
故答案为:$\frac{59W}{9aV}-5$.
点评 本题考查滴定操作、滴定应用与计算、物质组成含量测定等,难度中等,注意滴定中经常根据关系式进行计算,掌握根据关系式计算方法.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
1.下列物质属于碱的是( )
| A. | Na2CO3 | B. | NaOH | C. | HCl | D. | BaSO4 |
2.下列反应属于氧化还原反应的是( )
| A. | CaCO3═CaO+CO2↑ | B. | Na2CO3+2HCl═2NaCl+CO2↑+H2O | ||
| C. | 2Fe3++Cu═2Fe2++Cu2+ | D. | BaCl2+H2SO4═BaSO4↓+2HCl |
19.易拉罐主要为铝合金,其中以铝铁合金和铝镁合金最为常见.现取几小块易拉罐碎片进行下列实验,其中实验方案与现象、结论正确的是( )
| 序号 | 实验方案 | 现象 | 结论 |
| A | 加入盐酸 | 产生无色气体 | 含铝、铁、镁三种元素 |
| B | 加入NaOH溶液 | 产生无色气体 | 含有铝元素 |
| C | 加盐酸溶解后,再加入少量NaOH溶液 | 产生白色沉淀 | 含有镁元素 |
| D | 加盐酸溶解后,再滴加KSCN溶液 | 溶液呈血红色 | 含有铁元素 |
| A. | A | B. | B | C. | C | D. | D |
6.用己知浓度的NaOH溶液滴定未知浓度的醋酸,下列实验用品中一定不需要的是( )
| A. | 酸式滴定管 | B. | 碱式滴定管 | C. | 甲基橙 | D. | 酚酞 |
16.常温下,1.0mol/L一元酸HA与等体积等浓度KOH溶液混合,所得溶液粒子的浓度关系如表(不含水分子的5种粒子,A为短周期元素),下列说法正确的是( )
| 粒子 | K+ | A - | X | Y | Z |
| 浓度(mol/L) | 0.50 | 0.49 | c(X)>c(Y)>c(Z) | ||
| A. | 元素A最高价氧化物对应水化物为HAO4 | |
| B. | 表格中X表示HA,Y表示H+ | |
| C. | 所得溶液中c(X)+c(A-)=c(K+) | |
| D. | 等体积等浓度的HA和盐酸分别加水稀释10倍后,pH (HA)>pH(HCl) |
3.下列实验操作或装置(略去部分加持仪器)正确的是( )
| A. | 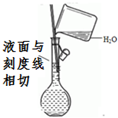 配制溶液 | B. | 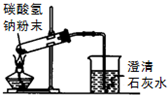 碳酸氢钠受热分解 | ||
| C. | 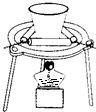 钠的燃烧 | D. | 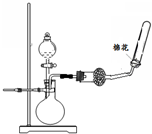 制取收集干燥的氨气 |
20.下列有关热化学方程式的叙述正确的是( )
| A. | 已知2H2 (g)+O2(g)═2H2O(g )△H=-483.6kJ/mol,则H2的燃烧热为△H=-241.8kJ/mol | |
| B. | 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4kJ/mol | |
| C. | 反应NH3(g)+HCl(g)═NH4Cl (s)△H<0,该反应在任何温度下都可自发进行 | |
| D. | 已知C(s)+O2(g)═CO2(g)△H1;C(s)+$\frac{1}{2}$O2(g)═CO(g)△H2,则△H1>△H2 |
1.设NA表示阿伏加德罗常数的值,下列结论中正确的是( )
| A. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| B. | 粗铜精炼时,当阳极质量减少6.4g时,电路中转移电子数一定不是0.2NA | |
| C. | 含0.2molH2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA | |
| D. | 200mL0.5mol/LNa2CO3溶液中,由于CO32-水解,所以阴离子数目小于0.1NA |