题目内容
18.下列依据热化学方程式得出的结论错误的是( )| A. | 已知HCl(aq)+NaOH(aq)=NaCl(aq)+H2O△H=-57.3kJ/mol,则含40gNaOH的稀溶液与足量稀醋酸完全中和放出的热量小于57.3kJ | |
| B. | 已知2H2O(l)=2H2(g)+O2(g)△H=+571.6kJ/mol-1,则氢气燃烧热为285.8 kJ/mol | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,则石墨比金刚石稳定 | |
| D. | 已知S(s)+O2(g)=SO2(g)△H1,S(g)+O2(g)=SO2(g)△H2,则△H1<△H2 |
分析 A.醋酸是弱酸存在电离平衡,电离过程是吸热过程;
B.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量;
C.物质能量越高,该物质越不稳定;
D.固态硫具有能量较低,则第一个反应放出热量减小,而焓变为负值,则△H1>△H2.
解答 解:A.醋酸是弱酸存在电离平衡,电离过程是吸热过程,则含40.0gNaOH物质的量为1mol的稀溶液与稀醋酸完全中和,放出的热量小于57.3KJ,故A正确;
B.已知2H2O(l)=2H2(g)+O2(g)△H=+571.6kJ/mol-1,则2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ/mol,说明1mol氢气完全燃烧生成稳定的氧化物放出的热量为285.8KJ,所以氢气的燃烧热为285.8 kJ/mol,故B正确;
C.物质能量越高越活泼,已知c(石墨,s)=C(金刚石,s)△H>0,石墨能量小于金刚石,则石墨比金刚石稳定,故C正确;
D.固体硫燃烧时要先变为气态硫,该过程吸热,气体与气体反应生成气体比固体和气体反应生成气体产生热量多,但反应热为负值,则△H1>△H2,故D错误;
故选D.
点评 本题考查了反应热与焓变的应用,题目难度中等,涉及燃烧热、中和热概念及物质稳定性比较,注意掌握反应热大小比较方法,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.青海昆仑玉的主要成分是由“透闪石”和“阳起石”组成的纤维状微晶结合体,透闪石(Tremolite)的化学成分为Ca2Mg5Si8O22(OH)2.下列有关说法不正确的是( )
| A. | 透闪石的化学式写成氧化物的形式为2CaO•5MgO•8SiO2•H2O | |
| B. | 透闪石中Mg的质量分数是Ca的质量分数的1.5倍 | |
| C. | 1molCa2Mg5Si8O22(OH)2与足量盐酸作用,至少需要14molHCl | |
| D. | 透闪石是一种新型无机非金属材料,难溶于水 |
6.已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是( )
| A. | 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=-4b kJ/mol | |
| B. | C2H2(g)+$\frac{5}{2}$O2(g) 2CO2(g)+H2O(l);△H=2b kJ/mol | |
| C. | 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=-2b kJ/mol | |
| D. | 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=b kJ/mol |
3.某元素原子的第三电子层上只有2个电子,该元素在周期表中的位置是( )
| A. | 第二周期ⅠA族 | B. | 第三周期ⅠA族 | C. | 第二周期ⅦA族 | D. | 第三周期ⅡA族 |
10.合理补充碘、铁元素是十分必要的,下列说法不正确的是( )
| A. | 为了补充碘而食用过多的加碘盐或含碘食品 | |
| B. | 如果体内缺铁,人就会患缺铁性贫血,儿童缺铁还可能导致智力发育迟缓 | |
| C. | 强化铁强化酱油,可以帮助预防缺铁性贫血 | |
| D. | 过量服用补铁剂可能引起铁中毒,造成胃肠道出血性坏死 |
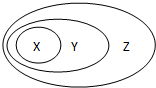 用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )
用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )