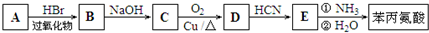题目内容
一定温度下密封容器中发生可逆反应:mA(g)+nB(g)?pC(g),达平衡后,若将气体体积压缩到原来的
.当再达平衡时C的浓度是原来的1.8倍,则下列叙述正确的是( )
| 1 |
| 2 |
| A、C气体的体积分数增大 |
| B、m+n>p |
| C、气体A的转化率升高 |
| D、平衡向逆反应方向移动 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:将气体体积压缩到原来的
,若平衡不移动,C的浓度应为原来的2倍,当再达平衡时C的浓度是原来的1.8倍,说明平衡逆向移动,据此解答.
| 1 |
| 2 |
解答:
解:将气体体积压缩到原来的
,若平衡不移动,C的浓度应为原来的2倍,当再达平衡时C的浓度是原来的1.8倍,说明平衡逆向移动,
A、平衡逆向移动,C的体积分数减小,故A错误;
B、减小容器体积,平衡逆向移动,说明m+n<p,故B错误;
C、平衡逆向移动,A的转化率减小,故C错误;
D、将气体体积压缩到原来的
,若平衡不移动,C的浓度应为原来的2倍,当再达平衡时C的浓度是原来的1.8倍,说明平衡逆向移动,故D正确;
故选D.
| 1 |
| 2 |
A、平衡逆向移动,C的体积分数减小,故A错误;
B、减小容器体积,平衡逆向移动,说明m+n<p,故B错误;
C、平衡逆向移动,A的转化率减小,故C错误;
D、将气体体积压缩到原来的
| 1 |
| 2 |
故选D.
点评:本题考查了将气体体积压缩到原来的
,气体的浓度变化引起的平衡移动,题目难度不大.
| 1 |
| 2 |

练习册系列答案
相关题目
如图所示,两个连通容器用活塞分开,左室容积为右室的两倍,但温度相同,现分别按如图所示的量充入气体,加入少量固体催化剂使左右两室内气体充分反应达到平衡,打开活塞,继续反应再次达到平衡,下列有关判断正确的是( )
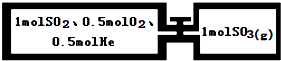

| A、通入气体未反应前,左室压强比右室大 |
| B、第一次平衡时,左室内压强一定小于右室 |
| C、第一次平衡时,SO2的物质的量右室更多 |
| D、第二次平衡时,SO2的总物质的量比第一次平衡时左室SO2的物质的量的2倍多 |
密闭容器中进行反应:A(g)+2B(g)═3C(g)+D(s),能说明该反应已达到化学平衡状态的是( )
| A、A、B、C、D物质的量之比为1:2:3:1 |
| B、压强不随时间变化而变化 |
| C、υ(A):υ(B):υ(C)=1:2:3 |
| D、A的体积分数不随时间变化而变化 |
处于平衡状态的反应2H2S(g)═2H2(g)+S2(g)△H>0,下列说法正确的是( )
| A、若体系恒容,通入H2S(g),则正反应速率增大,逆反应速率减小 |
| B、升高温度,正逆反应速率都增大,H2S分解率也增大 |
| C、增大压强,平衡向逆反应方向移动,将引起体系温度降低 |
| D、若体系恒容,注入一些H2后达新平衡,H2浓度将减小 |
下列说法正确的是( )
| A、常温下,在0.1mol/LNaOH溶液和0.1mol/L盐酸中水的离子积相等 |
| B、常温下,在水中加入NaOH,水的电离受到抑制,水的离子积减小 |
| C、HCl溶液中无OH-,NaOH溶液中无H+,NaCl溶液中既无OH-也无H+ |
| D、在水溶液中导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质 |
小红中午放学回家后,妈妈在高压锅内做了她最爱吃的鸡肉请问高压锅是下列什么合金制造的( )
| A、锰合金 | B、铝合金 |
| C、镍合金 | D、铁合金 |
下列选项中,与物质体积大小无关的因素是( )
| A、粒子数目 |
| B、粒子大小 |
| C、粒子之间的距离 |
| D、粒子的化学性质 |
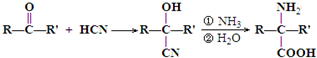
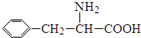 )是合成APM的原料之一.苯丙氨酸的一种合成途径如图所示:
)是合成APM的原料之一.苯丙氨酸的一种合成途径如图所示: