题目内容
7.海水中含有丰富的化学元素,下面是某化工厂从海水中提取化工原料及综合利用的生产流程简图: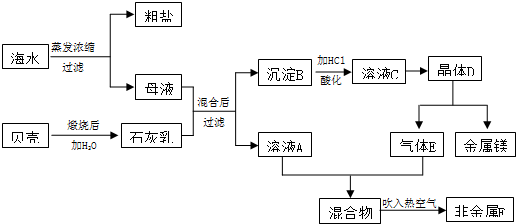
回答下列问题:
(1)从溶液C得到晶体D的过程,需要进行的实验操作依次为D E C(填写操作序号).
A.蒸馏 B.灼烧 C.过滤 D.蒸发 E.冷却结晶
(2)由晶体D获取气体E及金属镁还需要经过两步工艺,第一步制取无水盐,第二步采用熔融电解,写出第二步的反应方程式MgCl2$\frac{\underline{\;电解\;}}{\;}$ Mg+Cl2↑.有同学觉得为了减少步骤节约药品,提出如下的获取金属镁的方案你觉得是否可行否(填“是”或“否”).
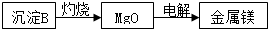
(3)由溶液A和气体E反应得到的非金属F是Br2(或液溴 或溴单质).
分析 海水经蒸发、结晶得到粗盐,煅烧贝壳生成氧化钙,氧化钙和水反应生成氢氧化钙,母液中含有氯化镁,加入氢氧化钙生成氢氧化镁,B为氢氧化镁,与盐酸反应生成氯化镁溶液,C为氯化镁溶液,将溶液进行蒸发、浓缩、过滤、干燥得到氯化镁,电解熔融的氯化镁可得到氯气、镁,E为氯气,氯气和溶液A反应可生成溴,用热空气吹,可得到溴,以此解答该题.
(1)从溶液C得到晶体D为氯化镁,需要进行的实验操作依次为蒸发、冷却结晶、过滤;
(2)氯化镁电解生成镁和氯气;氧化镁的熔点高,工业上是电解熔融的氯化镁制取镁;
(3)电解熔融的氯化镁可得到氯气、镁,E为氯气,氯气和溶液A反应可生成溴,用热空气吹,可得到溴.
解答 解:(1)母液中含有氯化镁,加入氢氧化钙生成氢氧化镁,B为氢氧化镁,Mg(OH)2中加入盐酸后,要获得MgCl2晶体,需要进行的实验操作为:蒸发浓缩,冷却结晶、过滤得到,
故答案为:DEC;
(2)氯化镁电解生成镁和氯气,反应为:MgCl2$\frac{\underline{\;电解\;}}{\;}$ Mg+Cl2↑,因为MgO熔点很高,能耗太大,不经济,所以利用氯化镁冶炼金属镁而不利用氧化镁,所以该同学获取金属镁的方案不可,
故答案为:MgCl2$\frac{\underline{\;电解\;}}{\;}$ Mg+Cl2↑;否;
(3)溴元素在海水中以Br-形式存在,电解熔融的氯化镁可得到氯气、镁,E为氯气,氯气和溶液A反应可生成溴,溴易挥发,升高温度促进其挥发,所以通入热空气的目的是吹出Br2,
故答案为:Br2(或液溴 或溴单质).
点评 本题考查了海水资源的综合利用,工业生产流程的分析判断,电解原理的应用,粗盐的提纯步骤,晶体的提纯方法,题目内容综合性较强,难度中等.

练习册系列答案
相关题目
18.下列有关高级脂肪酸甘油酯的说法不正确的是( )
| A. | 高级脂肪酸甘油酯是高分子化合物 | |
| B. | 天然的不饱和高级脂肪酸甘油酯都是混甘油酯 | |
| C. | 植物油可以使酸性高锰酸钾溶液褪色 | |
| D. | 油脂皂化完全后原有的液体分层现象消失 |
15.有关如图所示化合物的说法不正确的是( )
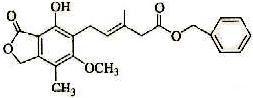

| A. | 一定条件下,既可以与Br2发生加成反应,又可以与Br2发生取代反应 | |
| B. | 1 mol该化合物最多可以与3 molNaOH反应 | |
| C. | 既可以催化加氢,又可以在稀硫酸存在下水解得2种有机物 | |
| D. | 可以与Na2CO3溶液反应放出CO2气体 |
2.一定条件下,可逆反应N2+3H2═2NH3△H<0 达到平衡后,只改变一个条件,下列叙述错误的是( )
| A. | 加催化剂,v正、v逆 都发生变化,且变化的倍数相等 | |
| B. | 加压,v正、v逆 都增大,且v正 增大的倍数大于V逆增大的倍数 | |
| C. | 增大氮气的浓度,N2的平衡转化率减小,H2的平衡转化率增大 | |
| D. | 降温,v正、v逆 都减小,且v正 减小的倍数大于v逆减小的倍数 |
13.下列有关表述正确的是( )
| A. | 次氯酸的电子式: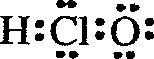 | B. | 硫原子的价电子排布式:3s23p4 | ||
| C. | 氮化硅的分子式:Si4N3 | D. | N原子的电子排布图为: |
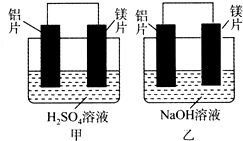 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol•L-1的H2SO4溶液中,乙同学将电极放入6 mol•L-1的NaOH溶液中,如图所示.
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol•L-1的H2SO4溶液中,乙同学将电极放入6 mol•L-1的NaOH溶液中,如图所示.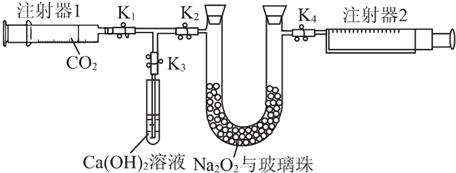
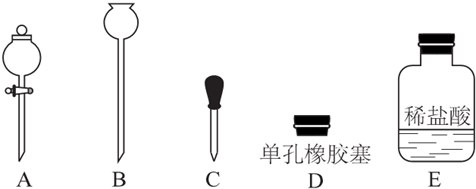
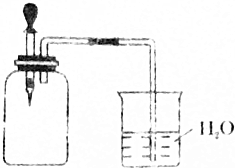 如图所示,将1molCH4与1molCl2混合后充入集气瓶内,置于光亮处,让混合气体缓慢地反应一段时间.
如图所示,将1molCH4与1molCl2混合后充入集气瓶内,置于光亮处,让混合气体缓慢地反应一段时间.