题目内容
实验室用120mL 10mol/L 的浓盐酸和MnO2 共热制取Cl2 ,生成标准状况下的Cl2 2.24L,试计算被氧化的HCl的物质的量和参加反应的MnO2 的质量.
考点:化学方程式的有关计算
专题:
分析:根据生成的氯气的物质的量结合化学方程式进行计算被氧化的HCl的物质的量和参加反应的MnO2 的质量.
解答:
解:标准状况下2.24L氯气的物质的量n=
=
=0.1mol,被氧化的氯化氢是氯气的2倍,所以被氧化的氯化氢为0.2mol,因为消耗二氧化锰的量和产生氯气的量之间的关系为:MnO2~Cl2↑,所以参加反应的MnO2的物质的量为0.1mol,质量m=nM=0.1mol×87g/mol=8.7g,
答:被氧化的氯化氢为0.2mol,参加反应的MnO2质量是8.7g.
| V |
| Vm |
| 2.24L |
| 22.4L/mol |
答:被氧化的氯化氢为0.2mol,参加反应的MnO2质量是8.7g.
点评:本题考查氧化还原反应的特征和实质以及化学方程式的计算知识,是对教材知识的考查,难度不大.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
 一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器中,发生如下反应:
一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器中,发生如下反应:A(g)+B(g)?x C(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C 的浓度随时间变化如图所示.下列说法正确是( )
| A、反应方程式中的x=1 |
| B、t1~t3间该反应的平衡常数均为4 |
| C、t3时刻改变的条件是移去少量物质D |
| D、t3时刻改变的条件是使用催化剂 |
按如图所示装置进行下列不同的操作,其中不正确的是( )
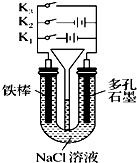

| A、只接通K1,一段时间后,U形管中出现白色沉淀 |
| B、只接通K2,U形管左、右两端液面均下降 |
| C、若U形管左、右两端上方充入一些空气,铁腐蚀的速度由大到小的顺序是:只接通K1>只接通K3>都断开>只接通K2 |
| D、若将氯化钠溶液改为氢氧化钠溶液,铁棒改为多孔石墨,先只接通K2,一段时间后,漏斗内液面上升,然后再只接通K3,则接通K3后装置中无电流通过 |
下列溶液中微粒的物质的量浓度关系正确的是( )
A、0.01mol?L-1HCl溶液与pH=12的氨水等体积混合:c(Cl-)>c(NH
| ||
B、0.1mol?L-1NaCO3溶液:C(OH-)=c(HCO
| ||
| C、已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中:c(Na+)-c(F-)=c(K+)-c(CH3COO-) | ||
| D、0.1mol?L-1CH3COOH溶液和0.1mol?L-1CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=c(CH3COOH)+2c(H+) |
下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A、0.1 mol?L-1 NaHB溶液 pH=4,则溶液中:c(HB-)>c(B2-)>c(H2B) |
| B、0.1 mol?L-1 (NH4)2Fe(SO4)2溶液中:c(NH4+)+c(Fe2+)=0.3 mol?L-1 |
| C、NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
| D、Na2CO3溶液中:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Na+) |
下列属于物理变化的是( )
| A、氯气溶于水 | B、食物变质 |
| C、焰色反应 | D、光合作用 |