题目内容
室温时,将20mL某气态烃与过量的氧气混合,充分燃烧后冷却至室温,发现混合气体的体积减少60mL,将所得混合气体通过氢氧化钠溶液后,体积又减少80mL.
(1)通过计算确定气态烃分子式
(2)若该烃能使溴水和高锰酸钾褪色,且该烃与H2加成后的产物有三个甲基,请写出该烃的结构简式.又知该烃在一定的温度、压强和催化剂的作用下,生成一种高聚物,写出其方程式.
(1)通过计算确定气态烃分子式
(2)若该烃能使溴水和高锰酸钾褪色,且该烃与H2加成后的产物有三个甲基,请写出该烃的结构简式.又知该烃在一定的温度、压强和催化剂的作用下,生成一种高聚物,写出其方程式.
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:(1)该气态烃的组成为CxHy,燃烧方程式为CxHy+(x+
)O2
xCO2+
H2O,NaOH溶液吸收80mL为燃烧生成CO2的体积,产物通过浓硫酸,再恢复至室温,气体体积减少了60mL,根据方程式利用差量法计算相互x、y,从而确定其分子式;
(2)根据该烃的化学性质及与氢气反应生成产物中含有3个甲基取代其结构简式,然后写出该烃发生加聚反应的化学方程式.
| y |
| 4 |
| 点燃 |
| y |
| 2 |
(2)根据该烃的化学性质及与氢气反应生成产物中含有3个甲基取代其结构简式,然后写出该烃发生加聚反应的化学方程式.
解答:
解:(1)NaOH溶液吸收80mL为燃烧生成CO2的体积,产物通过浓硫酸,再恢复至室温,气体体积减少了60mL,则:
CxHy+(x+
)O2
xCO2+
H2O 体积减小△V
1 (x+
) x 1+
20mL 80mL 60mL
故x=
=4,
1+
=
,则y=8,
所以该烃的分子式为C4H8,
答:气态烃的分子式为C4H8;
(2)该烃能使溴水和高锰酸钾褪色,则该烃分子中含有不饱和键,该烃为丁烯,与H2加成后的产物有三个甲基的丁烯为:2-甲基-1-丙烯,其结构简式为: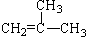 ;
;
2-甲基-1-丙烯发生加聚反应的化学方程式为:n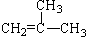
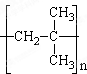 ,
,
答:该烃的结构简式为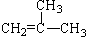 ;该烃发生加聚反应的方程式为:n
;该烃发生加聚反应的方程式为:n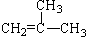
 .
.
CxHy+(x+
| y |
| 4 |
| 点燃 |
| y |
| 2 |
1 (x+
| y |
| 4 |
| y |
| 4 |
20mL 80mL 60mL
故x=
| 80mL×1 |
| 20mL |
1+
| y |
| 4 |
| 60mL×1 |
| 20mL |
所以该烃的分子式为C4H8,
答:气态烃的分子式为C4H8;
(2)该烃能使溴水和高锰酸钾褪色,则该烃分子中含有不饱和键,该烃为丁烯,与H2加成后的产物有三个甲基的丁烯为:2-甲基-1-丙烯,其结构简式为:
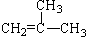 ;
;2-甲基-1-丙烯发生加聚反应的化学方程式为:n
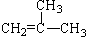
| 一定条件下 |
 ,
,答:该烃的结构简式为
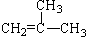 ;该烃发生加聚反应的方程式为:n
;该烃发生加聚反应的方程式为:n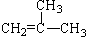
| 一定条件下 |
 .
.
点评:本题考查了有机物结构与性质、有机物分子式、结构简式的计算,题目难度中等,注意掌握确定有机物分子式、结构简式的方法,明确常见有机物结构与性质的关系,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
下列物质的主要成分正确的是( )
| A、赤铁矿:Fe3O4 |
| B、小苏打:NaHCO3 |
| C、磁铁矿:Fe2O3 |
| D、明矾:KAl(SO4)2 |
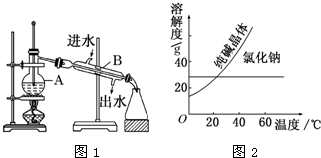 如图为实验室制取蒸馏水的装置示意图,回答下列问题:
如图为实验室制取蒸馏水的装置示意图,回答下列问题: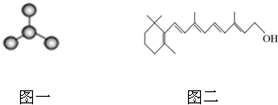 图一、图二表示两种有机物.
图一、图二表示两种有机物.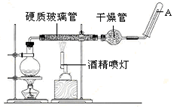 常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.