题目内容
6.下列关于有机物的叙述正确的是( )| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 分子式为C2H6O2且能与NaOH溶液反应的有机物一定是乙酸 | |
| C. | 油脂和纤维素都是能发生水解反应的高分子化合物 | |
| D. | 甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应 |
分析 A.乙烯与溴水发生加成反应,苯与溴水不反应;
B.分子式为C2H6O2且能与NaOH溶液反应,可能为酸或酯;
C.油脂的相对分子质量在10000以下;
D.甲烷、苯中的H可被取代,乙醇、乙酸的酯化反应和酯类的水解反应均为取代反应.
解答 解:A.乙烯与溴水发生加成反应,苯与溴水不反应,分别为化学变化、物理变化,原理不同,故A错误;
B.分子式为C2H6O2且能与NaOH溶液反应,可能为乙酸或甲酸甲酯,故B错误;
C.油脂的相对分子质量在10000以下,不是高分子,而淀粉为高分子,二者均可发生水解反应,故C错误;
D.甲烷、苯中的H可被取代,乙醇、乙酸的酯化反应和酯类的水解反应均为取代反应,则均可发生取代反应,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意高分子及同分异构体的判断,题目难度不大.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
16.某有机物的结构简式为 ,它在一定条件下可能发生的反应是( )
,它在一定条件下可能发生的反应是( )
①加成;②水解;③酯化;④氧化;⑤中和;⑥消去;⑦还原.
 ,它在一定条件下可能发生的反应是( )
,它在一定条件下可能发生的反应是( )①加成;②水解;③酯化;④氧化;⑤中和;⑥消去;⑦还原.
| A. | ①③④⑤⑦ | B. | ①③④⑤⑥⑦ | C. | ①③⑤⑥⑦ | D. | ②③④ |
17.徐光宪在《分子共和国》一书中介绍了许多明星分子,如H2O2、CO2、BF3、CH3COOH等.下列说法正确的是( )
| A. | H2O2分子的空间构型为直线形 | |
| B. | CO2分子为含有极性键的极性分子 | |
| C. | BF3分子中的B原子不满足8电子稳定结构 | |
| D. | CH3COOH分子中C原子均为sp2杂化 |
14.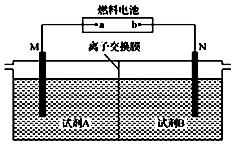 以二甲醚(CH3OCH3)酸性燃料电池为电源,电解饱和食盐水制备氯气和烧碱,设计装置如图所示.已知:a电扱的反应式为O2+4H++4e-═2H2O,下列说法不正确的是( )
以二甲醚(CH3OCH3)酸性燃料电池为电源,电解饱和食盐水制备氯气和烧碱,设计装置如图所示.已知:a电扱的反应式为O2+4H++4e-═2H2O,下列说法不正确的是( )
 以二甲醚(CH3OCH3)酸性燃料电池为电源,电解饱和食盐水制备氯气和烧碱,设计装置如图所示.已知:a电扱的反应式为O2+4H++4e-═2H2O,下列说法不正确的是( )
以二甲醚(CH3OCH3)酸性燃料电池为电源,电解饱和食盐水制备氯气和烧碱,设计装置如图所示.已知:a电扱的反应式为O2+4H++4e-═2H2O,下列说法不正确的是( )| A. | b电极的反应式为CH3OCH3+3H2O-12e-═2CO2↑+12H+ | |
| B. | 试剂A为饱和食盐水,试刑B为NaOH稀溶液 | |
| C. | 阳极生成1 mol气体时,有1mol离子通过离子交换膜 | |
| D. | 阴极生成1 mol气体时,理论上导线中流过2 mol e- |
1.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | |
| B. | 0.1mol${\;}_{38}^{90}$Sr原子中含中子数为3.8NA | |
| C. | 足量的O2与1molNa充分反应,转移的电子数为NA | |
| D. | 50mL12mol•L-1的盐酸与足量MnO2共热,转移电子数为0.3NA |
11.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=1的溶液:Na+、K+、MnO4-、SO42- | |
| B. | 0.1mol•L-1FeCl3溶液:K+、NH4+、I-、SCN- | |
| C. | 使酚酞变红色的溶液:Na+、Al3+、CO32-、Cl- | |
| D. | 由水电离的c(H+)=1×10-13mol•L-1的溶液:K+、Na+、AlO2-、CO32- |
18.短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的.由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生.下列说法不正确的是( )
| A. | X的简单氢化物的热稳定性比W强 | |
| B. | Y的简单离子与X的具有相同的电子层结构 | |
| C. | Y与Z形成的化合物的水溶液可使蓝色石蕊试纸变红 | |
| D. | Z与X属于同一主族,与Y属于同一周期 |
14.用电解氧化法可以在铝制品表面形成致密、耐腐蚀的氧化膜,电解质溶液一般为H2SO4-H2C2O4混合溶液.下列叙述错误的是( )
| A. | 待加工铝质工件为阳极 | |
| B. | 可选用不锈钢网作为阴极 | |
| C. | 阴极的电极反应式为:Al3++3e-═Al | |
| D. | 硫酸根离子在电解过程中向阳极移动 |
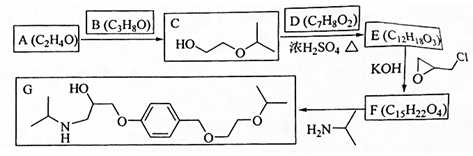
 .
.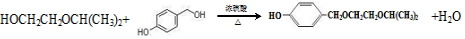 .
.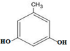 、
、 .
.