题目内容
5.氧化还原滴定实验与中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之).现用0.001mol•L-1 KMnO4酸性溶液滴定未知浓度的无色NaHSO3溶液.反应的离子方程式是2MnO4-+5HSO3-+H+=2Mn2++5SO42-+3H2O填空完成问题:
(1)该滴定实验所需仪器有下列中的ADEFH.
A酸式滴定管(50mL) B碱式滴定管(50mL) C量筒(10mL) D锥形瓶 E铁架台 F滴定管夹 G烧杯 H白纸 I胶头滴管 J漏斗
(2)不能用碱(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液.试分析原因酸性KMnO4溶液会腐蚀碱式滴定管下端胶管.
(3)选何种指示剂,说明理由不用指示剂,高锰酸钾溶液颜色为紫红色,滴定终点时,溶液由无色变为红色.
分析 (1)酸性高锰酸钾具有强氧化性,实验时应用酸式滴定管,无色NaHSO3溶液显酸性,用酸式滴定管,滴定过程还需要烧杯、锥形瓶、白纸、滴定管夹和铁架台;
(2)高锰酸钾具有强氧化性能腐蚀碱式滴定管中的橡胶管;
(3)高锰酸钾溶液颜色为紫红色,可不用加入指示剂.
解答 解:(1)酸性高锰酸钾具有强氧化性,实验时应用酸式滴定管,无色NaHSO3溶液显酸性,用酸式滴定管,滴定过程还需要锥形瓶盛放待测液、白纸对比终点颜色变化、滴定管夹和铁架台,所以需要用到的是:ADEFH,
故答案为:ADEFH;
(2)高锰酸钾具有强氧化性能腐蚀碱式滴定管中的橡胶管,所以不用用碱式滴定管盛放高锰酸钾溶液,应该用酸式滴定管;
故答案为:碱;酸性KMnO4溶液会腐蚀碱式滴定管下端胶管;
(3)高锰酸钾溶液颜色为紫红色,滴定终点时,溶液由无色变为红色,不用指示剂,当最后一滴溶液滴入,溶液的紫色退去,且30s内不复现,可达到滴定终点,
故答案为:不用指示剂,高锰酸钾溶液颜色为紫红色,滴定终点时,溶液由无色变为红色.
点评 本题考查中和滴定知识以及误差分析,侧重于学生的分析能力、实验能力的考查,注意把握实验的方法和操作,难度中等.

练习册系列答案
相关题目
15.S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的方法有2种:①CS2+3Cl2$\stackrel{50-60℃}{→}$CCl4+S2Cl2;②2S+Cl2$\stackrel{95-100}{→}$S2Cl2.已知S2Cl2中硫元素显+1价,电子式: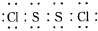 ,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).反应涉及的几种物质的熔沸点如表:
,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).反应涉及的几种物质的熔沸点如表:
实验室利用下列装置制备S2Cl2(部分夹持仪器已略去).回答下列问题:
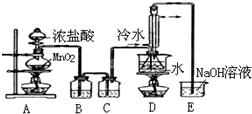
(1)写出A装置中发生反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸的理由是稀盐酸还原性弱,反应困难.
(3)D中冷凝管起到导气和冷凝回流双重作用.这种冷却装置可应用于下列高中化学中ACD实验.
A.石油分馏 B.制备乙烯
C.制取乙酸乙酯 D.制取溴苯
(4)B装置中盛放的是饱和食盐水,反应结束后从锥形瓶内混合物中分离出产品的方法是蒸馏,D中采用热水浴加热的原因是使CS2平稳汽化,避免产物S2Cl2汽化.
(5)A装置仪器装配时,整套装置装配完毕后,应先进行气密性检查,再添加试剂.实验完毕,拆除装置时,应先将E中长导管移开液面,目的是防止倒吸.
(6)实验过程中,若缺少C装置,则发现产品浑蚀不清,出现该现象的原因可用化学方程式表示为2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑.实验完毕,当把剩余浓盐酸倒人E烧杯中与吸收了尾气的氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是ClO-+2H++Cl-=Cl2↑+H2O.(用离子方程式表示)
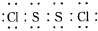 ,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).反应涉及的几种物质的熔沸点如表:
,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).反应涉及的几种物质的熔沸点如表:| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |

(1)写出A装置中发生反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸的理由是稀盐酸还原性弱,反应困难.
(3)D中冷凝管起到导气和冷凝回流双重作用.这种冷却装置可应用于下列高中化学中ACD实验.
A.石油分馏 B.制备乙烯
C.制取乙酸乙酯 D.制取溴苯
(4)B装置中盛放的是饱和食盐水,反应结束后从锥形瓶内混合物中分离出产品的方法是蒸馏,D中采用热水浴加热的原因是使CS2平稳汽化,避免产物S2Cl2汽化.
(5)A装置仪器装配时,整套装置装配完毕后,应先进行气密性检查,再添加试剂.实验完毕,拆除装置时,应先将E中长导管移开液面,目的是防止倒吸.
(6)实验过程中,若缺少C装置,则发现产品浑蚀不清,出现该现象的原因可用化学方程式表示为2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑.实验完毕,当把剩余浓盐酸倒人E烧杯中与吸收了尾气的氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是ClO-+2H++Cl-=Cl2↑+H2O.(用离子方程式表示)
13.一定温度下,在三个体积都为2L的恒容密闭容器中发生反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)
回答下列问题:
(1)反应的△H<O (填“>”或“<”);判断的理由是投料量相同时,温度高的容器,平衡时二甲醚的物质的量小,说明反应为放热反应,△H小于0.
(2)容器I到达平衡所需的时间为20s,反应速率v(CH3OH)为0.004mol/(L•s).390℃时该反应的平衡常数K1=4(填数值).
(3)容器II达平衡时,压强是容器I的两倍,CH3OH的体积分数和容器I中的相同,CH3OH起始的物质的量为0.40mol;平衡时CH3OH(g)的体积分数为20%.
(4)390℃,若向3L容器中充入0.9mol CH3OH(g),0.6mol CH3OCH3(g)和0.3molH2O(g),则起始时该反应速率V正>V逆.(填“>”“<”或“=”)
| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| Ⅰ | 390 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 390 | |||
| Ⅲ | 230 | 0.20 | 0.090 | 0.090 |
(1)反应的△H<O (填“>”或“<”);判断的理由是投料量相同时,温度高的容器,平衡时二甲醚的物质的量小,说明反应为放热反应,△H小于0.
(2)容器I到达平衡所需的时间为20s,反应速率v(CH3OH)为0.004mol/(L•s).390℃时该反应的平衡常数K1=4(填数值).
(3)容器II达平衡时,压强是容器I的两倍,CH3OH的体积分数和容器I中的相同,CH3OH起始的物质的量为0.40mol;平衡时CH3OH(g)的体积分数为20%.
(4)390℃,若向3L容器中充入0.9mol CH3OH(g),0.6mol CH3OCH3(g)和0.3molH2O(g),则起始时该反应速率V正>V逆.(填“>”“<”或“=”)
10.对已达到化学平衡的反应2A(g)+3B(s)?2C(g),增大压强时,对反应产生的影响是( )
| A. | 正反应速率增大,逆反应速率减小,平衡向正向移动 | |
| B. | 逆反应速率增大,正反应速率减小,平衡逆向移动 | |
| C. | 正、逆反应速率都增大,平衡不移动 | |
| D. | 正、逆反应速率都增大,平衡向正反应方向移动 |
17.以NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 58.5 g氯化钠固体中含有NA个氯化钠分子. | |
| B. | 1 mol Fe参与反应失去电子数目一定为2NA | |
| C. | 1 molNA被完全氧化生成Na2O2,失去2NA个电子 | |
| D. | 常温下,46 g NO2和N2O4的混合物中含有的氮原子数为NA |
14.随着人们生活节奏的加快,方便的小包装食品已被广泛接受,为了防止副食品氧化变质,延长食品的保质期,在包装袋中常放入抗氧化物质.下列不属于抗氧化物质的是( )
| A. | 生石灰 | B. | 亚硫酸钠(Na2SO3) | C. | 铁粉 | D. | 硫酸亚铁(FeSO4) |
15.下列实验设计能完成或实验结论合理的( )
| 操作及现象 | 结 论 | |
| A | 用蒸馏水润湿的pH试纸测溶液的pH | 一定会使测定结果偏低 |
| B | 向硅酸钠溶液中,滴入硫酸 | 可以验证S的氧化性强于Si |
| C | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
| D | 向含有少量FeBr2的FeCl2溶液中,加入适量氯水,再加CCl4萃取分液 | 除去FeCl2溶液中的FeBr2 |
| A. | A | B. | B | C. | C | D. | D |