题目内容
4.下列是利用烃C3H6合成有机高分子E和烃C6H14的流程图.请回答以下问题: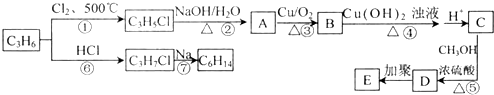
(1)①〜⑥中属于取代反应的有①②⑤;
(2)写出E的结构简式
 ;
;(3)写出B与新制Cu(OH)2悬浊液反应的化学方程式:CH2=CHCHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH2=CHCOONa+Cu2O↓+3H2O;
(4)D的同分异构体很多,符合下列条件的同分异构体有3种,其中氢原子核磁共振谱谱峰最少的结构简式为
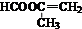 .
.①含碳碳双键 ②能水解 ③能发生银镜反应
(5)根据你所学知识和上图中相关信息,以乙醇为主要原料通过三步可以合成环己烷(无机试剂任选),写出反应的流程图(有机物质写结构简式).
分析 烃C3H6与HCl反应生成C3H7Cl,则烃C3H6为CH2=CHCH3,CH2=CHCH3与氯气在加热条件下生成C3H5Cl,应是发生取代反应,C3H5Cl在氢氧化钠水溶液、加热条件下发生水解反应生成A,而A可以连续发生氧化反应,故C3H5Cl为CH2=CHCH2Cl,A为CH2=CHCH2OH,B为CH2=CHCHO,C为CH2=CHCOOH,C与甲醇发生酯化反应生成D为CH2=CHCOOCH3,D发生加聚反应生成E为 .CH2=CHCH3与HCl发生加成反应生成C3H7Cl,C3H7Cl在Na条件下生成C6H14,应属于取代反应,据此解答.
.CH2=CHCH3与HCl发生加成反应生成C3H7Cl,C3H7Cl在Na条件下生成C6H14,应属于取代反应,据此解答.
解答 解:烃C3H6与HCl反应生成C3H7Cl,则烃C3H6为CH2=CHCH3,CH2=CHCH3与氯气在加热条件下生成C3H5Cl,应是发生取代反应,C3H5Cl在氢氧化钠水溶液、加热条件下发生水解反应生成A,而A可以连续发生氧化反应,故C3H5Cl为CH2=CHCH2Cl,A为CH2=CHCH2OH,B为CH2=CHCHO,C为CH2=CHCOOH,C与甲醇发生酯化反应生成D为CH2=CHCOOCH3,D发生加聚反应生成E为 .CH2=CHCH3与HCl发生加成反应生成C3H7Cl,C3H7Cl在Na条件下生成C6H14,应属于取代反应.
.CH2=CHCH3与HCl发生加成反应生成C3H7Cl,C3H7Cl在Na条件下生成C6H14,应属于取代反应.
(1)反应①②⑤属于取代反应,反应③④属于氧化反应,反应⑥属于加成反应,
故答案为:①②⑤;
(2)由上述分析可知,E的结构简式为: ,
,
故答案为: ;
;
(3)B(CH2=CHCHO)与新制Cu(OH)2悬浊液反应的化学方程式:CH2=CHCHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH2=CHCOONa+Cu2O↓+3H2O,
故答案为:CH2=CHCHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH2=CHCOONa+Cu2O↓+3H2O;
(4)D(CH2=CHCOOCH3)的同分异构体很多,符合下列条件的同分异构体:①含碳碳双键 ②能水解,含有酯基,③能发生银镜反应,应含有甲酸形成的酯基,符合条件的同分异构体有:CH2=CHCH2OOCH、
、CH3CH=CHOOCH、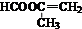 ,氢原子核磁共振谱谱峰最少的结构简式为:
,氢原子核磁共振谱谱峰最少的结构简式为: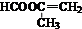 ,
,
故答案为:3;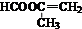 ;
;
(5)先在浓硫酸、加热170℃条件下发生消去反应生成乙烯,乙烯与溴发生加成反应生成1,2-二溴乙烷,根据转化中反应⑦可知,1,2-二溴乙烷与Na发生反应生成环己烷与NaBr,合成路线流程图为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2 $\stackrel{Br_{2}}{→}$ BrCH2CH2Br$\stackrel{Na}{→}$  ,
,
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2 $\stackrel{Br_{2}}{→}$ BrCH2CH2Br$\stackrel{Na}{→}$  .
.
点评 本题考查有机物的推断也合成,注意根据有机物分子式与反应条件推断,需要学生熟练掌握官能团的性质与转化,较好的考查学生的分析推理能力,(5)中注意根据转化中隐含的信息进行设计,难度中等.

 一本好题口算题卡系列答案
一本好题口算题卡系列答案| A. | 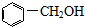 醇类-OH 醇类-OH | |
| B. | CH3CH2CH2COOH 羧酸-COOH | |
| C. | 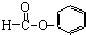 醛类-CHO 醛类-CHO | |
| D. | CH3-O-CH3 醚类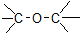 |
| A. | 铝表面有一层致密的氧化物薄膜,故铝制容器可用来腌制咸菜等 | |
| B. | 如果发生氯气泄漏,附近人员应迅速远离液氯泄漏地点,并顺风往低洼区域疏散 | |
| C. | “低碳生活”倡导生活中尽量减少耗能,从而减少CO2排放 | |
| D. | 向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 |
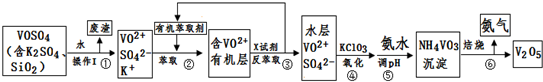
请回答下列问题:
(1)步骤①所得废渣的成分是SiO2(写化学式),操作I的名称过滤.
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):R2(SO4)n(水层)+2nHA(有机层)?2RAn(有机层)+nH2SO4(水层)
②中萃取时必须加入适量碱,其原因是加入碱中和产生的酸,平衡右移提高了钒的萃取率.
③中X试剂为硫酸.
(3)④的离子方程式为NH3•H2O+VO3-═NH4VO3↓+OH-.
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<2.6×10-3.
(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(5)该工艺流程中,可以循环利用的物质有有机萃取剂和氨气.
| A. | 按系统命名法,化合物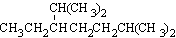 的名称为2,6-二甲基-5-乙基庚烷 的名称为2,6-二甲基-5-乙基庚烷 | |
| B. | 苯和油脂均不能使酸性KMnO4溶液褪色 | |
| C. | 有机物X的蒸气相对氢气的密度为51,X中氧元素的质量分数为31.7%,则能在碱性溶液中发生反应的X的同分异构体有(不考立体异构)13种 | |
| D. | 检验卤代烃中的卤素原子种类的方法是:加入NaOH溶液共热,再加AgNO3溶液,观察沉淀颜色 |
| A. | 同周期元素的电子层数都相同 | |
| B. | 同主族元素的最外层电子数不一定相同 | |
| C. | 最外层电子数相同的元素都在同一族 | |
| D. | 周期表是按相对原子质量逐渐增大的顺序从左到右排列的 |
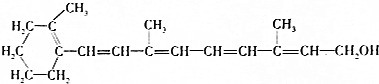 维生素A1是一切健康上皮组织必需的物质,缺乏维生素A1时会引起儿童发育不良,导致夜盲症、皮肤干燥等.已知维生素A1的结构简式如图:下列有关维生素A1的叙述错误的是( )
维生素A1是一切健康上皮组织必需的物质,缺乏维生素A1时会引起儿童发育不良,导致夜盲症、皮肤干燥等.已知维生素A1的结构简式如图:下列有关维生素A1的叙述错误的是( )| A. | 维生素A1中含有两种官能团 | |
| B. | 维生素A1的分子式为C18H26O | |
| C. | 维生素A1可使酸性KMnO4溶液褪色 | |
| D. | 维生素A1分子中含有苯环,1mol维生素A1最多可与7molH2发生加成反应 |
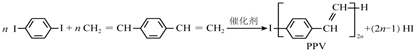
下列说法正确的是( )
| A. | 合成PPV的反应为加聚反应 | |
| B. | PPV与聚苯乙烯具有相同的重复结构单元 | |
| C. |  和苯乙烯互为同系物 和苯乙烯互为同系物 | |
| D. | 1mol 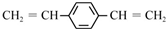 最多可以和5mol氢气发生加成反应 最多可以和5mol氢气发生加成反应 |
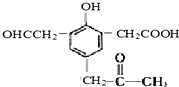 ,试回答:
,试回答: