题目内容
19.联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料.回答下列问题:(1)联氨是一种常用的还原剂,向装有少量AgBr的试管中加入联氨溶液,观察到的现象是固体逐渐变黑,并有气泡产生.
(2)联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀,理论上1kg的联氨可除去水中溶解的O21kg.
(3)与使用Na2SO3处理水中溶解的O2相比,联氨的优点是N2H4的用量少,不产生其他杂质(反应产物为N2和H2O),而Na2SO3产生Na2SO4.
分析 (1)联胺被银离子氧化,银离子被还原生成单质银,-2价的N元素被氧化为N2;
(2)联胺被氧化失电子N2H4~N2失4e-,O2→O2-得到4e-,依据得失电子守恒计算;
(3)依据锅炉的质地以及反应产物性质解答.
解答 解:(1)联胺被银离子氧化,银离子被还原生成单质银,-2价的N元素被氧化为N2,反应方程式为:N2H4+4AgBr=4Ag↓+N2↑+4HBr,因此反应出现现象为:固体逐渐变黑,并有气泡产生,故答案为:固体逐渐变黑,并有气泡产生;
(2)联胺被氧化失电子N2H4~N2,O2→O2-得到4e-,联胺和氧气摩尔质量都是32g/mol,则等质量联胺和氧气物质的量相同,理论上1kg的联氨可除去水中溶解的O21kg,故答案为:1;
(3)由于肼的氧化产物是氮气,不会对锅炉造成腐蚀,而亚硫酸钠被氧化产物为硫酸钠,易生成硫酸盐沉淀影响锅炉的安全使用,与使用Na2SO3处理水中溶解的O2相比,联氨的优点是用量少,不产生其他杂质(反应产物为N2和H2O),而Na2SO3产生Na2SO4,
故答案为:N2H4的用量少,不产生其他杂质(反应产物为N2和H2O),而Na2SO3产生Na2SO4.
点评 本题考查了氮及其化合物性质,主要是氧化还原反应的计算及其产物的判断,题目难度中等.

练习册系列答案
相关题目
7.根据热化学方程式:S(g)+O2(g)═SO2(g)△H=-Q kJ•mol-1(Q>0),则下列分析正确的是( )
| A. | 1mol S(g) 与1mol O2(g)的总能量比1mol SO2(g)的总能量低Q kJ | |
| B. | 1mol S(g) 与1mol O2(g)反应生成1mol SO2(g)放出Q kJ 的能量 | |
| C. | S(s)+O2(g)═SO2(g)△H<-Q kJ•mol-1 | |
| D. | 1个 S(g) 与1个 O2(g)完全反应可放出 Q kJ的能量 |
6.碳酸镍可用于电镀、陶瓷器着色等.镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS(含有Fe、Cu、Ca、Mg、Zn等元素杂质),从镍矿渣出发制备碳酸镍的流程如下:
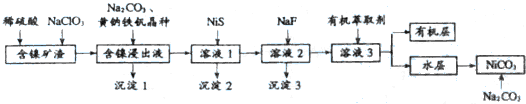
已知:(Ⅰ)含镍浸出液的成分及离子沉淀的pH:
(Ⅱ)溶度积常数:
(1)镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS,写出浸取时反应的离子方程式3NiS+4ClO3-=3Ni2++3SO42-+4Cl-或3NiS+ClO3-+6H+=3Ni2++3S+Cl-+3H2O.
(2)黄钠铁钒[NaFe3(SO4)2(OH)6]具有沉淀颗粒大、沉淀速度快,容易过滤等特点,常用于除铁.写出流程中第一次加入 Na2CO3溶液时反应的离子方程式:Na++3Fe3++2SO42-+3H2O+3CO32-=NaFe3(SO4)2(OH)6↓+3CO2↑;
(3)NiS的作用是除去溶液中的Cu2+,原理是NiS+Cu2+═CuS+Ni2+,该反应的平衡常数是8.43×104;
(4)滤液2中加入NaF的作用是除去溶液中的Ca2+、Mg2+,则加入NaF先沉淀的离子是Mg2+.
(5)NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由NiCO3为原料获得,结合上述流程,制备NiSO4•6H2O的操作步骤如下:
①向被有机萃取剂萃取后所得的水层中加入足量Na2CO3溶液(流程中第二次加Na2CO3溶液),搅拌,得NiCO3沉淀:
②过滤,并用蒸馏水洗涤沉淀2-3次直至流出液用pH试纸检验呈中性;
③向沉淀中加6mol/L的H2SO4溶液,直至恰好完全溶解;
④蒸发、冷却结晶并从溶液中分离出晶体;
⑤用少量乙醇洗涤并晾干.
确定步骤①中Na2CO3溶液足量,碳酸镍己完全沉淀的简单方法是:上层清液呈无色(或静置后向上层液中再加入Na2CO3溶液后没有沉淀生成);
补充完整上述步骤②和③【可提供的试剂有6mol/L的H2SO4溶液,蒸馏水、pH试纸】.

已知:(Ⅰ)含镍浸出液的成分及离子沉淀的pH:
| 元素 | Na2+ | Fe3+ | Cu2+ | Ca2+ | Mg2+ | Zn2- |
| 浓度/g•L-1 | 5.25 | 0.47 | 0.30 | 0.40 | 0.18 | 0.81 |
| 开始沉淀PH | 6.4 | 2.2 | 4.7 | / | 9.6 | 6.5 |
| 完全沉淀PH | 8.4 | 3.5 | 6.7 | / | 11.6 | 8.5 |
| 难溶物 | NiS | CuS | ZnS | |
| 溶度积常数 | 1.07×10-21 | 1.27×10-26 | 2.93×10-25 | |
| 难溶物 | CaF2 | MgF2 | ZnF2 | NiF2 |
| 溶度积常数 | 1.46×10-10 | 7.42×10-11 | 3.04×10-2 | 微溶 |
(2)黄钠铁钒[NaFe3(SO4)2(OH)6]具有沉淀颗粒大、沉淀速度快,容易过滤等特点,常用于除铁.写出流程中第一次加入 Na2CO3溶液时反应的离子方程式:Na++3Fe3++2SO42-+3H2O+3CO32-=NaFe3(SO4)2(OH)6↓+3CO2↑;
(3)NiS的作用是除去溶液中的Cu2+,原理是NiS+Cu2+═CuS+Ni2+,该反应的平衡常数是8.43×104;
(4)滤液2中加入NaF的作用是除去溶液中的Ca2+、Mg2+,则加入NaF先沉淀的离子是Mg2+.
(5)NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由NiCO3为原料获得,结合上述流程,制备NiSO4•6H2O的操作步骤如下:
①向被有机萃取剂萃取后所得的水层中加入足量Na2CO3溶液(流程中第二次加Na2CO3溶液),搅拌,得NiCO3沉淀:
②过滤,并用蒸馏水洗涤沉淀2-3次直至流出液用pH试纸检验呈中性;
③向沉淀中加6mol/L的H2SO4溶液,直至恰好完全溶解;
④蒸发、冷却结晶并从溶液中分离出晶体;
⑤用少量乙醇洗涤并晾干.
确定步骤①中Na2CO3溶液足量,碳酸镍己完全沉淀的简单方法是:上层清液呈无色(或静置后向上层液中再加入Na2CO3溶液后没有沉淀生成);
补充完整上述步骤②和③【可提供的试剂有6mol/L的H2SO4溶液,蒸馏水、pH试纸】.
4.在U形管中用惰性电极电解硫酸钠和石蕊的混合液,一段时间后,可以观察到的现象是( )
| A. | 两极附近颜色无明显变化 | B. | 两极产生等量气体 | ||
| C. | 阳极附近的颜色变红 | D. | 阴极附近的颜色变红 |
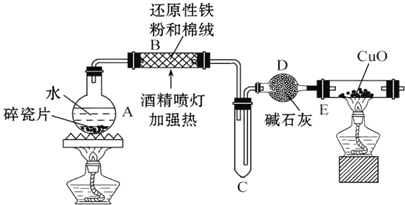 某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题: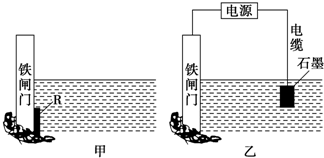 下面两个图都是金属防护的例子.
下面两个图都是金属防护的例子.