题目内容
下列说法正确的是
| A.利用SO2的漂白性可使酸性高锰酸钾溶液褪色 |
| B.漂白粉既可做漂白棉麻纸张的漂白剂,又可做游泳池及环境的消毒剂 |
| C.为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质 |
| D.为增强漂白效果,可将等物质的量的SO2和Cl2混合使用以达到增强效果的目的 |
B
解析试题分析:A、SO2具有还原性,能使酸性高锰酸钾溶液褪色,与SO2的漂白性无关系,A不正确;B、漂白粉的有效成分是次氯酸钙,漂白粉既可做漂白棉麻纸张的漂白剂,又可做游泳池及环境的消毒剂,B正确;C、氯气没有漂白性,真正起漂白剂作用的是氯气与水反应生成的次氯酸,因此液氯没有漂白性,C不正确;D、SO2具有还原性,氯气具有强氧化性,等物质的量的SO2和Cl2混合后发生反应SO2+Cl2+2H2O=H2SO4+2HCl,所以失去漂白性,D不正确,答案选B。
考点:考查常见漂白剂的有关判断和应用

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱和NaCl 溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
| B | 向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X 中一定含有SO42- |
| C | 用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中 | 出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
| D | 向浓度均为0. 1 mol·L-1 NaCl 和NaI 混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
下列有关试剂的保存方法,错误的是
| A.金属钠保存在煤油中 |
| B.存放FeSO4溶液时加入少量铁粉 |
| C.NaOH溶液保存在带胶塞的玻璃试剂瓶中 |
| D.新制的氯水保存在无色广口瓶中 |
化学与生产、生活密切相关。下列叙述中,正确的是( )
| A.制作计算机芯片的材料是SiO2晶体,84消毒液的有效成分是NaClO |
| B.水在4℃时主要以(H2O)2存在,两个水分子间可能以某种特殊的分子间作用力相结合 |
| C.0.2摩尔铝和足量氢氧化钠溶液反应,参加还原反应的水是3.6克 |
| D.SO2和CO2都能使雨水的pH < 5.6,造成酸雨 |
下列物质的转化在给定条件下能实现的是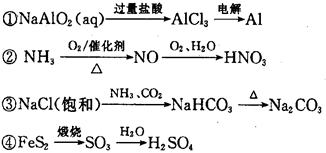
| A.②③ | B.①④ | C.②④ | D.③④ |
下列有关物质性质的应用正确的是
| A.液氨汽化时要吸收大量的热,可用作制冷剂 |
| B.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 |
| C.生石灰能与水反应,可用来干燥氯气 |
| D.氯化铝是一种电解质,可用于电解法制铝 |
下列说法正确的是
| A.在2H2O2 =2H2O +O2反应中,每生成32g氧气,则转移2NA个电子 |
| B.钠、铁的金属性均比铜的强,说明两者均可以从硫酸铜溶液中置换出单质铜 |
| C.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| D.将SO2通入品红溶液,溶液褪色后加热恢复原色;将氨气通入酚酞溶液中,变色后加热不能恢复原色 |
下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是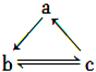
| | a | b | c |
| A | Al | AlCl3 | Al(OH)3 |
| B | HNO3 | NO | NO2 |
| C | S | SO3 | H2SO4 |
| D | Si | SiO2 | H2SiO3 |
下列叙述I和II均正确并且有因果关系的是
| 选项 | 叙述I | 叙述II |
| A | 相同条件下NaHCO3的溶解度比Na2CO3的小 | 向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊 |
| B | 钠比铜的金属性强 | 金属钠可从硫酸铜溶液中置换出铜单质 |
| C | 常温下铝与浓硫酸、浓硝酸均不反应 | 可用铝槽车密封运送浓硫酸、浓硝酸 |
| D | 合成氨反应为吸热反应 | 该反应需在高温条件下进行 |