题目内容
合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是( )
①采用较高温度(400℃~500℃)
②采用较高压强(20MPa~50MPa)
③用铁触媒加快化学反应速率
④将生成的氨液化并及时从体系中分离出来.
①采用较高温度(400℃~500℃)
②采用较高压强(20MPa~50MPa)
③用铁触媒加快化学反应速率
④将生成的氨液化并及时从体系中分离出来.
| A、①② | B、①③ | C、②④ | D、③④ |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动,使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答:
解:①合成氨反应为放热反应,升高温度不利用平衡向正方向移动,但升温却可提高反应速率,催化剂活性大,与勒沙特列原理不符,故①不符合;
②反应是气体体积减小的反应,加压平衡正向进行符合化学平衡移动原理,可以用勒夏特列原理解释,故②符合;
③用铁触媒加快化学反应速率,是利用铁触媒做催化剂降低反应的活化能,加快反应速率,不改变化学平衡,不能用勒夏特列原理解释,故③不符合;
④将生成的氨液化并及时从体系中分离出来,减少生成物浓度,平衡正向进行,可以用勒夏特列原理解释,故④符合;
综上所述②④正确;
故选C.
②反应是气体体积减小的反应,加压平衡正向进行符合化学平衡移动原理,可以用勒夏特列原理解释,故②符合;
③用铁触媒加快化学反应速率,是利用铁触媒做催化剂降低反应的活化能,加快反应速率,不改变化学平衡,不能用勒夏特列原理解释,故③不符合;
④将生成的氨液化并及时从体系中分离出来,减少生成物浓度,平衡正向进行,可以用勒夏特列原理解释,故④符合;
综上所述②④正确;
故选C.
点评:本题考查了化学平衡影响因素的分析判断,反应特征和平衡移动原理是解题关键,题目较简单.

练习册系列答案
相关题目
用于净化汽车尾气的反应:2NO(g)+2CO(g)?2CO2(g)+N2(g),已知297℃时,该反应速率极慢,平衡常数为1×1059.下列说法正确的是( )
| A、提高尾气净化效率的最好方法是升高温度 |
| B、装有尾气净化装置的汽车排出的气体中一定不含NO或CO |
| C、297℃时该反应正向进行的程度很大,故使用催化剂并无实际意义 |
| D、提高尾气净化效率的最佳途径是研制高效催化剂 |
下列有机物命名正确的是( )
A、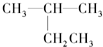 ,2-乙基丙烷 ,2-乙基丙烷 |
| B、(CH3)2CH-异丙基 |
C、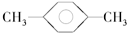 间二甲苯 间二甲苯 |
D、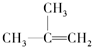 2-甲基-2-丙烯 2-甲基-2-丙烯 |
某可逆反应过程的能量变化如图所示,下列说法正确的是( )
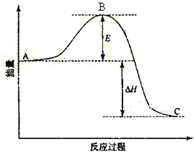

| A、该反应过程为吸热反应 |
| B、若加入催化剂,B点会降低 |
| C、若加入催化剂,△H数值会减小 |
| D、若升高温度,则平衡向正反应方向移动 |
下列各组微粒中,互为同位素的是( )
| A、金刚石和石墨 | ||||
B、
| ||||
| C、D2O和H2O | ||||
D、
|
下列说法正确的是(NA为阿伏加德罗常数的值)( )
| A、标准状况下,2.24L的水的物质的量为0.1mol |
| B、标准状况下,2.24 L Cl2溶于水中达到饱和,可得到HClO分子的数目是0.1NA |
| C、10.0 g CaCO3和KHCO3的混合物中含有氧原子数为0.3NA |
| D、2.3 g Na与氧气完全反应,反应中转移的电子数介于0.1 NA到0.2NA之间 |
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).能判断该反应是否达到化学平衡状态的依据是( )
| A、容器中压强不变 |
| B、单位时间内消耗了n mol CO2,同时生成了n mol H2O |
| C、v正(H2)=v逆(H2O) |
| D、c(CO2)=c(CO) |
某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3:1.用石墨作电极电解该混合溶液时,根据电极产物,可明显分为三个阶段.下列叙述不正确的是( )
| A、阴极自始自终只析出H2 |
| B、阳极先析出O2,后析出C12 |
| C、电解最后阶段为电解水 |
| D、溶液pH不断增大,最后为7 |