题目内容
下列各项中表达正确的是( )
A、F-的结构示意图: |
| B、CO2是由非极性共价键形成的分子 |
| C、NaCl的电子式为 Na:Cl: |
| D、N2的结构式为:N≡N: |
考点:电子式、化学式或化学符号及名称的综合,原子结构示意图,极性分子和非极性分子
专题:
分析:A.氟离子的核电荷数为9,核外电子总数为10,最外层达到8电子稳定结构;
B.二氧化碳中存在两个碳氧双键,碳氧键为极性键;
C.氯化钠为离子化合物,其电子式需要标出所带电荷;
D.氮气的结构式中不需要标出未成键电子对.
B.二氧化碳中存在两个碳氧双键,碳氧键为极性键;
C.氯化钠为离子化合物,其电子式需要标出所带电荷;
D.氮气的结构式中不需要标出未成键电子对.
解答:
解:A.氟离子的核电荷数为9,最外层达到8电子稳定结构,氟离子结构示意图为: ,故A正确;
,故A正确;
B.二氧化碳是由极性键形成的非极性分子,故B错误;
C.氯化钠为离子化合物,钠离子直接用电子式表示,阴离子需要标出所带电荷及最外层电子,氯化钠正确的电子式为: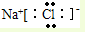 ,故C错误;
,故C错误;
D.氮气中存在氮氮三键,用短线代替所有的共用电子对即为结构式,氮气正确的结构式为:N≡N,故D错误;
故选A.
 ,故A正确;
,故A正确;B.二氧化碳是由极性键形成的非极性分子,故B错误;
C.氯化钠为离子化合物,钠离子直接用电子式表示,阴离子需要标出所带电荷及最外层电子,氯化钠正确的电子式为:
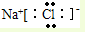 ,故C错误;
,故C错误;D.氮气中存在氮氮三键,用短线代替所有的共用电子对即为结构式,氮气正确的结构式为:N≡N,故D错误;
故选A.
点评:本题考查了电子式、离子结构示意图、结构式等化学用语的判断,题目难度中等,注意掌握常见化学用语的概念及表示方法,明确离子结构示意图与原子结构示意图、离子键与共价键的电子式的区别,试题考查了学生规范答题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
为防止碳素钢菜刀生锈,在使用后特别是切过咸菜后,应将其( )
| A、洗净、擦干 |
| B、浸泡在水中 |
| C、浸泡在食醋中 |
| D、直接置于空气中 |
氢化钠(NaH)是一种白色的离子化合物,其中钠元素显+1价;氢化钠与水反应放出氢气.下列叙述中,不正确的是( )
| A、NaH中存在-1价的氢离子,还原性比氢原子强 |
| B、NaH与H2O反应时水作氧化剂 |
| C、NaH中氢元素的离子的电子层排布与氦原子的电子层排布相同 |
| D、微粒半径:H+>H>H- |
 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A、W元素的第一电离能小于Y元素的第一电离能 |
| B、Y、Z的阴离子电子层结构都与R原子的相同 |
| C、p亚层未成对电子最多的是Z元素 |
| D、X元素是电负性最大的元素 |

 ,B、C可形成离子化合物B3C2,据此填空:
,B、C可形成离子化合物B3C2,据此填空: 铝和氢氧化钾都是重要的工业铲平.请回答:
铝和氢氧化钾都是重要的工业铲平.请回答: